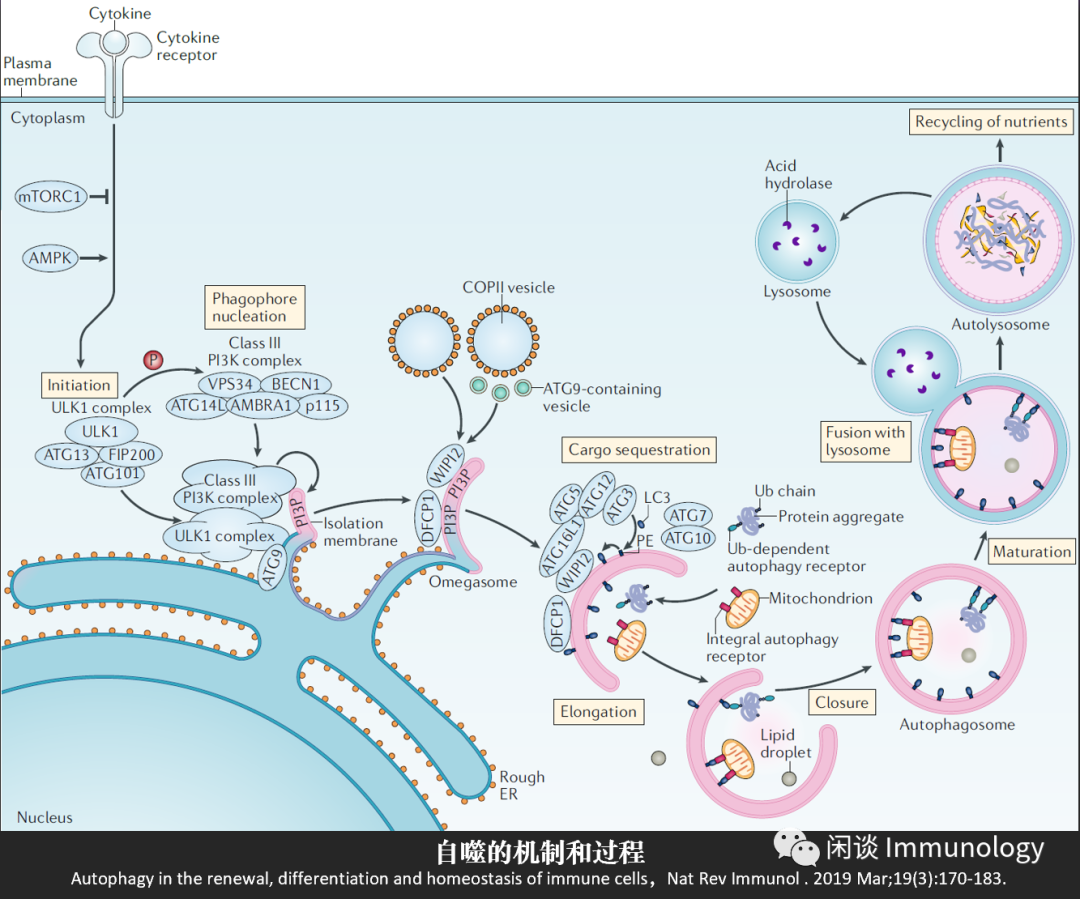
自噬是一种高度进化保守的机制, 用于细胞质的回收,降解和重利用。细胞质的一部分被双层膜包裹,形成自噬体,他们吞噬Cargo,与溶酶体融合,内容物被降解回收。
自噬可被一些列因素激活:氧气和养分供应的变化,激素、细胞因子、生长因子和受体结合,启动细胞分化或从静息状态退出。
一系列蛋白及蛋白复合物参与了此过程,具体见下图,不做赘述。
从造血干细胞,静息的免疫细胞,活化记忆免疫细胞,到浆细胞的免疫细胞稳态,都需要自噬参与维持。
选择性自噬
选择性自噬,通过适配器蛋白选择性靶向自噬体特定底物来实现。
适配器蛋白包括LC3相互作用结构域(LIR)和一个通常结合泛素的靶受体。
线粒体自噬(Mitophagy)
线粒体是细胞的能量中心,通过氧化磷酸化,三羧酸循环等产生ATP。线粒体自噬是线粒体的选择性降解,发生在损伤和发育过程中。
脂滴自噬(Lipophagy)
脂滴自噬是脂滴通过自噬降解的过程。脂滴是高密度的能量储存体,根据细胞对能量的需求发生动态重塑,通过自噬,脂滴被传递给溶酶体,发生降解。
此外还有内质网自噬体和核糖体自噬体等。
非典型自噬
自噬的一个亚类,没有完整的自噬体原件,一些自噬体的蛋白用于修饰膜。免疫系统相关的是LC3相关自噬(LC3- associated phagocytosis,LAP),高度依赖rubicon蛋白。rubicon和PI3K结合,启动LAP。也还有一些其他的非典型自噬。
自噬与免疫细胞分化和功能
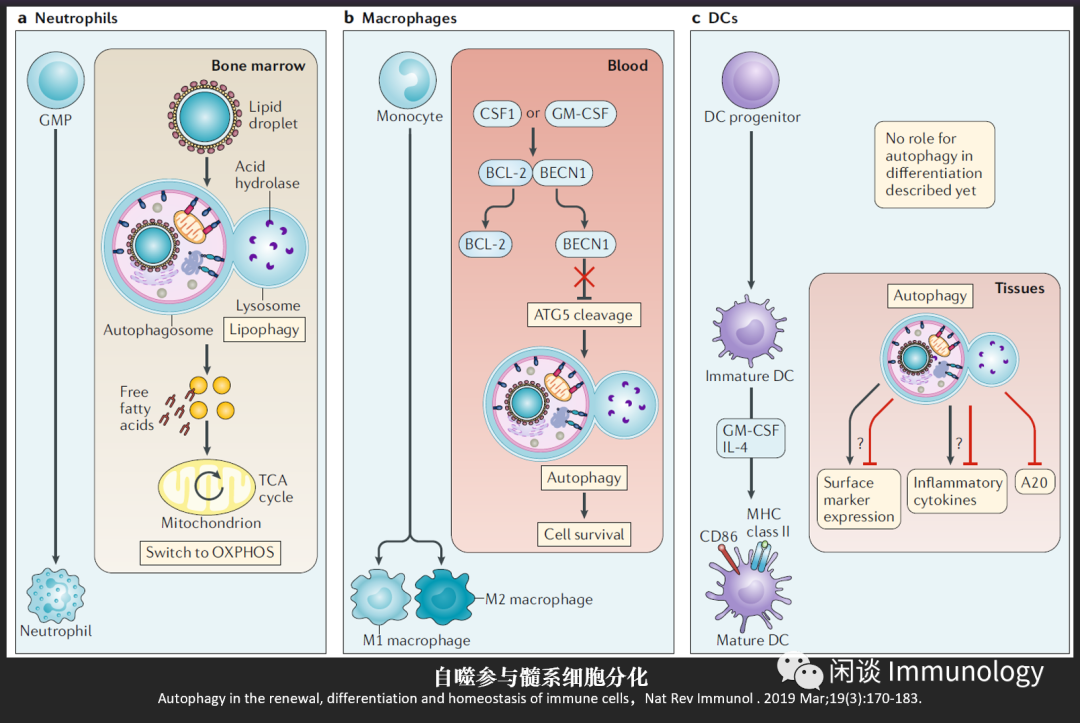
自噬与髓系细胞分化
中性粒细胞 从粒细胞-单核细胞祖细胞(GMPs)分化而来,依赖脂滴自噬(脂噬)来提供游离脂肪酸,以帮助满足从糖酵解到氧化磷酸化(OXPHOS) (涉及三羧酸(TCA)的要求)周期) 的能量需求。
巨噬细胞 从单核细胞分化而来,信号来自于集落刺激因子1(CSF1)和粒细胞-巨噬细胞集落刺激因子(GM-CSF),导致BECL1从BCL-2中释放。自噬蛋白5(ATG5)被剪切,信号不再被阻断,自噬的信号发生,促进分化巨噬细胞的存活。
未成熟DCs 成熟为免疫刺激DCs,受GM-CSF和IL-4诱导, 需要自噬参与。此过程中DC成熟的负性调节因子A20降解,此过程中共刺激因子CD80/CD86,促炎症因子(TNF,IL-1β),通过自噬增加或减少。
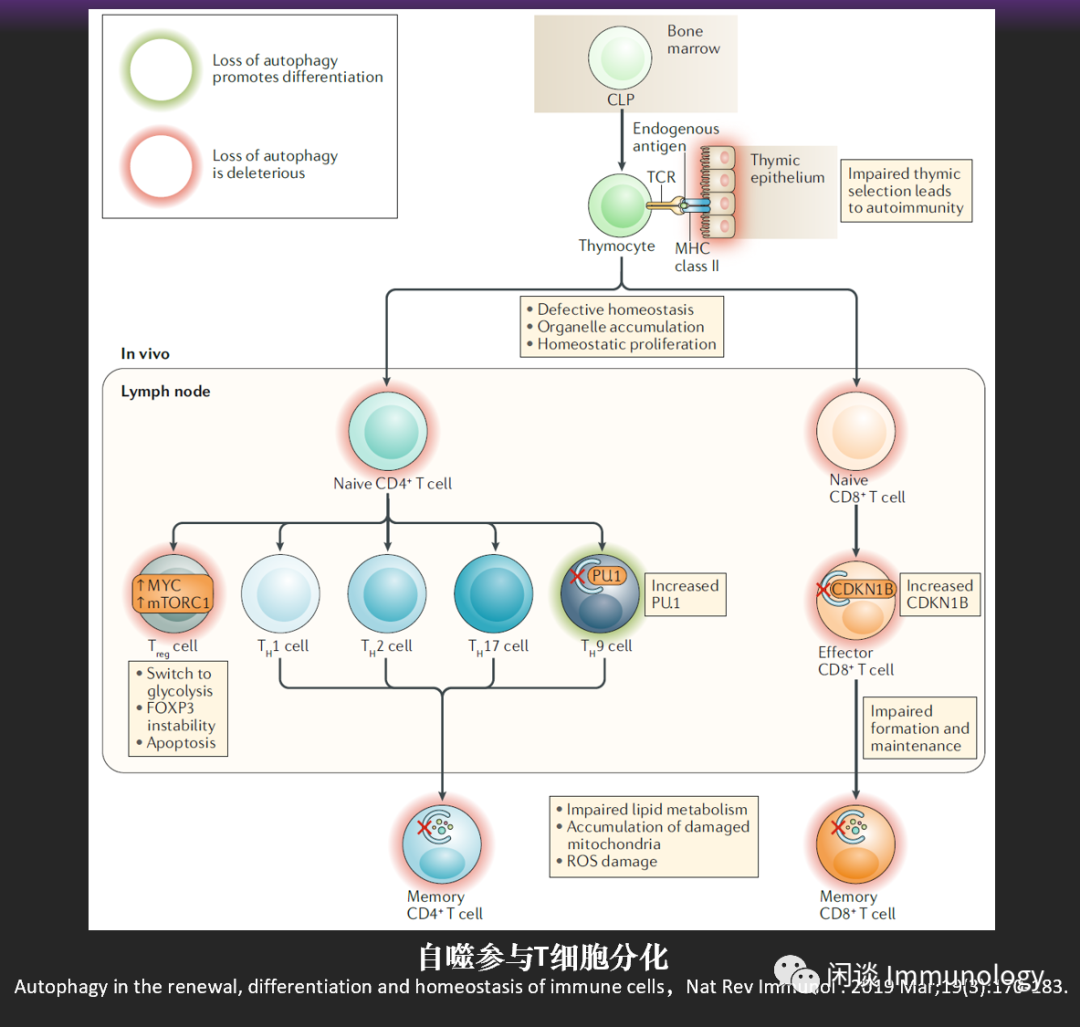
自噬与T细胞分化和功能
共同淋巴祖细胞进入胸腺,进入T细胞分化,其中胸腺上皮通过自噬,交叉递呈自身抗原-MHC II复合物,阴性选择自身反应性T细胞。
缺少自噬,容易形成TH9辅助T细胞亚群,因为其关键转录因子PU.1的降解,需要自噬参与。
自噬缺陷时,Treg的分化和维持也会发生缺陷,因为此时MYC,mTORC1激活,引起代谢转换为糖酵解,FOXP3不稳定和Treg的凋亡。
CD8+T细胞遭遇到抗原,自噬的缺陷,有助于CDKN18稳定和增加,促进效应功能的执行。
而CD4+T细胞记忆,也有赖于自噬的缺陷引起线粒体功能障碍,脂质代谢障碍。
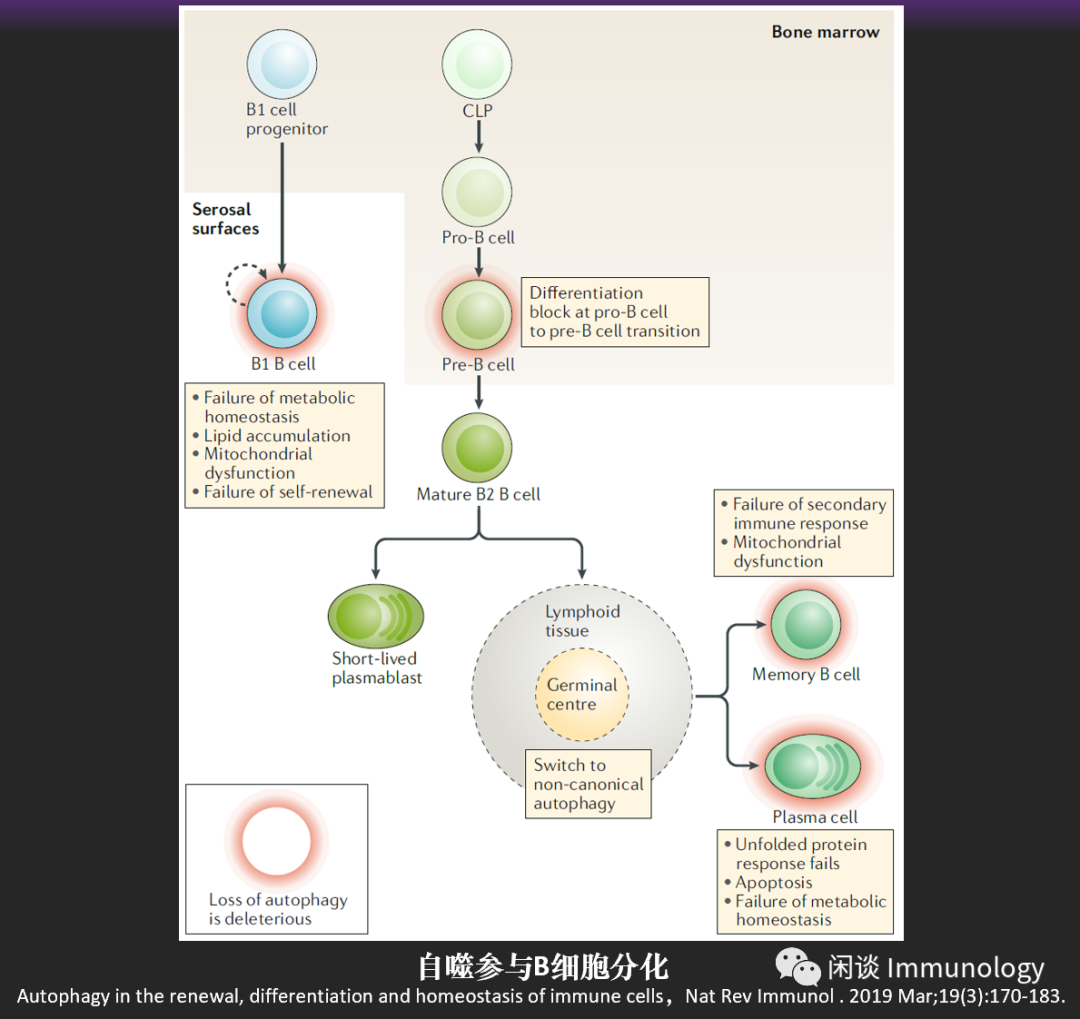
自噬参与B细胞分化
B细胞可以分为天然免疫样的B1细胞和B2细胞。
B1细胞存在于绒毛膜表面,在胎儿产生。自噬的缺陷,导致线粒体功能缺陷(线粒体自噬和脂质自噬缺陷),代谢稳态失调,脂质累积。所以这群细胞虽然分化正常,但是缺少自我更新能力,随着人体老化,逐渐减少。
在胚胎肝脏,缺乏自噬时,从Pro-B向Pre-B发育时,B2分化阻滞。
活化的B细胞 ,进入生发中心,在那里,他们从经典的自噬,转变为非经典的自噬,他们能够因此分化为长寿的浆细胞和记忆B细胞,如果自噬破坏,则影响浆细胞和记忆B细胞的形成。
浆细胞 产生抗体,因而是一个蛋白大量形成的细胞,依赖自噬来补充大量未折叠的蛋白质。缺乏自噬,内质网中错误折叠蛋白质增多,引起细胞凋亡。
记忆B细胞 在没有自噬的情况下形成,但是线粒体功能异常,形成大量活性氧中间产物,形成毒性。第二次抗体反应被破坏。