抗癌神药PD-1/PD-L1有哪些不良反应及应对方法
随着PD1/PD-L1单抗为代表的免疫治疗药物接连获批上市,应用患者越来越多,也带来了意想不到的生存获益。
与传统放化疗不同,免疫药物激发自身的免疫细胞杀伤肿瘤,整体不良反应较为温和,尽管其耐受性良好,3-4级严重不良反应少见,然而,由于体内激活的T细胞攻击力增强,在某些意外的情况下,也可能会攻击自身组织细胞,造成一系列自身免疫性炎症。
通过从JCO(《临床肿瘤学》)、TheOncologist(《肿瘤学》)、TheLancet(《柳叶刀》)、NEJM(《新英格兰医学期刊》)等全球权威医疗学术期刊上搜集数据,我们对PD-1/PD-L1抑制剂的副作用以及副作用的应对方式进行了整理。
免疫相关不良反应(irAEs)的常见类型:疲乏、无力、食欲下降、恶心、皮疹
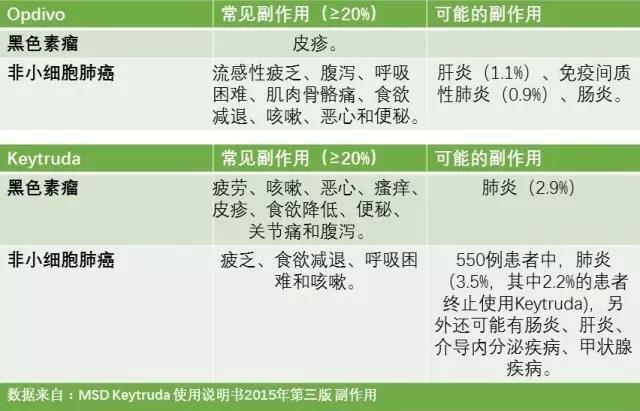
免疫相关不良反应(irAEs)或许归因于免疫抑制剂作用机制,由于增加的免疫活性或过度的免疫激活产生。主要的不良反应如下:
乍一看好像不良反应很多,但其实较为常见的副作用,仅为:疲乏、无力、食欲下降、恶心、皮疹。以下是PD-1/PD-L1常见不良反应及处理方法。
No.1
皮肤毒性
1级:
可不进行治疗或局部外用糖皮质激素、口服止痒剂(例如抗组胺药物,NK-1受体抑制剂等);可持续免疫治疗。
2级:
可在改善后恢复免疫治疗,但若连续治疗12周后病情仍无改善,则应停止免疫治疗。
3级:
应暂停PD-1抑制剂,并请皮肤科会诊行皮肤病学评估,包括临床评估、皮肤活检等,治疗上口服泼尼松,必要时静脉给药治疗,直到毒性严重程度≤1级。如果48h内恶化,考虑加用免疫抑制剂(如英夫利昔单抗,环磷酰胺,霉酚酸酯)。
No.2
腹泻与结肠炎
1级(每天<4次):
对症予以结肠炎饮食和胃肠动力抑制剂(洛派丁胺或复方地芬诺酯)。调整饮食并应用止泻药2~3d后症状仍持续但无加重时可应用布地奈德。
2级(每天4~6次):
一旦镜下明确结肠炎应暂停PD-1/PD-L1抗体,立即予以糖皮质激素治疗。
3级或4级(每天7次及以上或伴有并发症):
永久停用免疫检查点抑制剂治疗,并予以大剂量糖皮质激素。如果应用糖皮质激素3d后症状仍无改善者,推荐每2周加用一次英夫利昔单抗。对英夫利昔单抗耐药的患者可应用麦考酚酯。
No.3
肝脏毒性
1级(无症状,ALT或AST≤2.5xULN;总胆红素≤1.5xULN):
·行肝功能监测(LFT)直至恢复正常。
·如持续无症状,可继续应用抗PD1治疗。
2级(2.5xULN<ALT或AST≤5xULN;1.5xULN总胆红素≤3xULN):
·需排除其他病毒性肝炎及药物引起的肝炎。
·暂停抗PD1治疗,给予口服泼尼松或等量的激素治疗。
·每日监测LFT。
3-4级(ALT或AST>5xULN总胆红素>3xULN):
·放射学评估是否由肿瘤进展引起。
·停用抗PD-1治疗。
·给予甲强龙静脉点滴或等量激素治疗。
·每日监测LFT。
No.4
免疫治疗相关性肺炎
轻度:
采取对症药物治疗,如口服强的松或甲泼尼龙。
中度:
停用PD-1受体抑制剂,给予口服或静脉注射激素治疗。
重度:
首先停用PD-1受体抑制剂,严重的永久终止免疫治疗,并行支气管镜检查,请呼吸科医生会诊,以除外肺部感染和恶性肿瘤肺转移可能。
持续应用大剂量的皮质激素,如甲泼尼龙,必要时还需联合应用免疫抑制剂,如霉酚酸酯、环磷酰胺、英夫利昔单抗。
No.5
内分泌系统毒性
1级甲减:
应监测游离三碘甲腺原氨酸(fT3)和游离甲状腺素(fT4)。
2级甲减:
应用L-甲状腺素替代治疗,有症状的2级甲亢应优先使用甲巯咪唑治疗,必要时应用β受体阻滞剂。
3级甲减:
给予泼尼松龙。
4级甲减:
需要紧急停止PD-1抗体治疗并给予泼尼松龙。
No.6
PD-1/PD-L1阻断剂其它罕见毒性
肾脏毒性:
治疗上,均对类固醇激素治疗反应较好,早发现早诊断及时予以激素为主的治疗,可使血肌酐迅速下降避免透析治疗。
胰腺毒性:
若发现单纯胰酶水平的升高而没有其他症状怀疑胰腺炎时,可以监测指标变化并注意观察临床症状;必要时行MRI检查有助于早期诊断。
如果有腹痛等临床症状且酶升高水平较明显时,建议先停用PD-1抑制剂,并给予静脉激素治疗(甲强龙)。必要时请专科医师协助诊治。
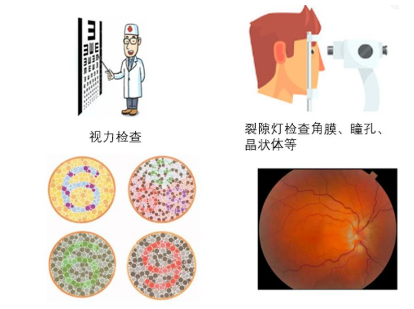
眼部毒性:
请眼科医师完善专科检查,外用类固醇滴眼可缓解症状。较重的眼科炎症推荐使用口服类固醇。
关节炎:
低剂量口服类固醇可有效控制症状。
神经系统疾病:
使用糖皮质激素可有效缓解毒副反应,并及时请神经科医师协助诊治。另外,也有推荐静脉应用免疫球蛋白或血浆置换。
其他irAEs还包括疲乏、心肌炎、胃炎、结节病、葡萄膜炎、风湿性多肌痛、脱髓鞘、血管炎、粒细胞减少等造血系统综合征等:
轻中度可行保守对症治疗,3/4级或迁延不愈的2级不良反应需停用PD-1抗体,并应用糖皮质激素治疗改善症状。
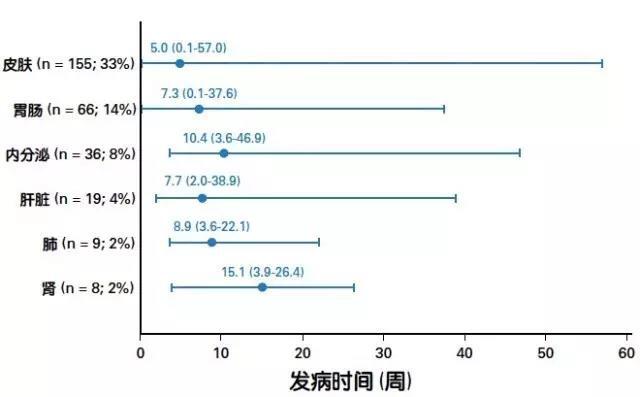
免疫相关不良反应(irAEs)的出现时间
大多数副作用不会在治疗的前四周出现。另外,对于不同的免疫相关毒性出现似乎有可预测模式。毒性作用出现时间一般来说是:皮肤>胃肠炎>肝脏>肺炎>内分泌>肾脏毒性。皮肤毒性通常用药后2-3周开始出现,胃肠道毒性通常用药后5周左右出现,肝脏和内分泌毒性通常用药后6-7周出现。
因为不良反应停药后,还能继续免疫治疗吗?
中断治疗后,患者一方面希望继续接受免疫治疗控制病情,另一方面又担心不良反应卷土重来。
中断后如何继续免疫治疗呢?
在临床试验中,不良事件发生后,医生一般会基于对受试者的安全性考量,不会贸然对出现严重毒性的患者恢复免疫治疗,更多的是改变治疗手段或采用维持治疗。
如果有指征可以继续治疗,医生会结合不良事件的类型、严重程度以及患者对免疫抑制治疗的情况,综合考虑是否再次使用免疫疗法。重新使用免疫疗法。
大致有如下三种方案:
在不同机制的免疫检查点抑制剂之间直接替换,目前临床有两类免疫检查点抑制剂:抗PD-(L)1(O药、K药)及抗CTLA-4药物(伊匹单抗),更换使用,一项临床试验显示,先前抗CTLA-4药物伊匹单抗治疗出现药物相关不良反应后,换用PD-1抗体,发现除垂体炎以外,所有的不良反应均解决;
在不良反应显著减弱后,重新引入同类药物或同一种免疫治疗药物,
一项临床试验中,患者接受免疫联合治疗后,发生严重毒性反应导致停药,待毒性作用减轻后,继续使用PD-1单药治疗。结果发现,仍有一半患者在进行不同程度的治疗后,出现了相关不良反应,包括18%具有严重毒性,30%患者再次停用抗PD1。
引入免疫抑制疗法,与免疫检查点抑制剂同时使用,降低不良反应风险。
重度不良事件患者再挑战的建议
在常规实践中,重度不良事件患者通常选择永久停药,如果患者发生严重的心血管,神经/肌肉或其他真正威胁生命的不良反应,应更谨慎的恢复免疫疗法。
如果恢复,建议医生密切监测病情进展,及时识别和处理复发/明显的不良事件,并根据临床提示及时停用免疫疗法。
所以,免疫治疗停药后,应在经验丰富的临床多学科团队指导下,个体化评估风险和受益,选择合理的治疗路径。
目前,PD1/PD-L1药物在国内临床应用日渐广泛,药物的毒副管理成为每一位临床医生必修科目。免疫药物与传统放、化疗的直接杀伤不同,依靠激发自身的免疫细胞杀伤肿瘤,3~4级的不良反应维持在10%左右,相比化疗的40%以上,整体不良反应较为温和,且以乏力、皮疹、消化道反应为主。但是,免疫治疗也存在一些特殊的不良作用,一旦忽视,也会出现严重不良后果,需要引起医生和患者重视。
在精准医学时代,免疫治疗对患者个性化管理的要求也更高,在这方面中国临床肿瘤学会(CSCO)也相继推出了《CSCO免疫检查点抑制剂相关的毒性管理指南》以及《CSCO免疫检查点抑制剂临床应用指南》以便更好地协助临床医生管理免疫治疗的用药以及不良反应处理,从而保证患者安全。