1994年,学者们提出了蛋白质组学的概念,此后蛋白质组学及其相关技术迅速发展,在癌生物学的研究中逐渐得到了广泛的应用。研究者使用各种蛋白分离技术,如二维凝胶电泳、液相色谱串联质谱(LC-MS)等技术手段筛选新的癌症生物标志物的潜在靶蛋白,为早期诊断和治疗提供重要依据。目前应用较为广泛的方法是非标记定量(label-free)蛋白质组学技术,它是通过液质联用技术对蛋白质酶解肽段进行质谱分析,该技术不需要使用昂贵的稳定同位素标签做内部标准,只需分析大规模鉴定蛋白质时所产生的质谱数据,比较不同样品中相应肽段的信号强度,从而对肽段对应的蛋白质进行相对定量。本文针对非标记蛋白组学技术在癌症研究中的应用做了解读。
案例一

中文标题:蛋白基因组学特征确定肝内胆管癌的临床亚型
研究对象:肝内胆管癌
发表期刊:Cancer Cell
运用技术:基因组学、转录组学、非标记蛋白质组学、磷酸化蛋白质组学
● 研究背景
肝内胆管癌(iCCA)是常见的原发性肝脏恶性肿瘤。多数患者发现时已是晚期,且治疗效果有限。因此迫切需要更深入地了解肝内胆管癌的发病机制以鉴定可能的治疗靶点。本文在国际癌症蛋白质基因组联盟(ICPC)的主持下,对262名中国iCCA患者进行了基因组学、转录组学、蛋白质组学、磷酸化蛋白质组学等分析,为进一步的生理病理研究、疾病诊断和药物研发提供基础数据。
● 研究思路
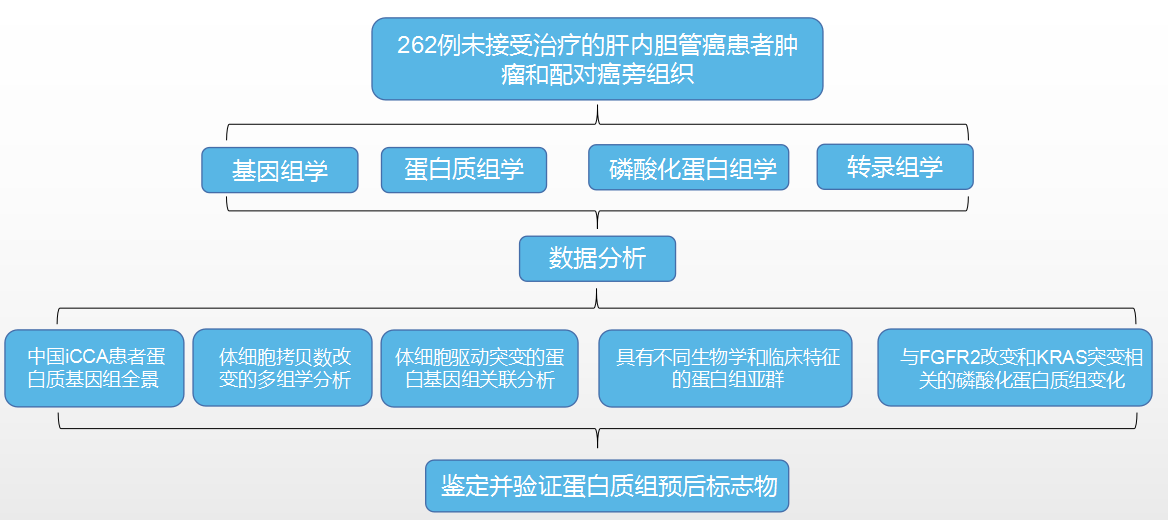
● 研究结果
为了描述中国iCCA患者的蛋白质基因组特征,作者收集了262个来自前瞻性队列的未接受治疗的iCCA患者肿瘤和配对癌旁组织(FU-iCCA)。共鉴定了12,197个非同义体细胞点突变和603个插入缺失。蛋白质组定量到了10,529种蛋白质,磷酸化蛋白质组定量到了来自9,832个磷酸化蛋白的62,879个磷酸化位点。基因组确定了包括TP53、KRAS、FGFR2、IDH1/2、BAP1、ARID1A和PBRM1在内的16个显著改变的肿瘤驱动基因(图1A)。与西方iCCA人群队列相比,本文队列显示出更高的KRAS突变频率和更低的IDH1、ARID1A和TERT突变频率(图1B)。在FU-iCCA队列中观察到黄曲霉毒素和马兜铃酸特征(图1C)。通过比较具有或不具有黄曲霉毒素特征的所有肿瘤的多组学数据,发现具有黄曲霉毒素特征的肿瘤显示出DNA修复和细胞周期通路的上调以及细胞凋亡、感染炎症和免疫通路的下调(图1E)。进一步分析显示,TP53突变与黄曲霉毒素特征显著相关(图1F和1G)。
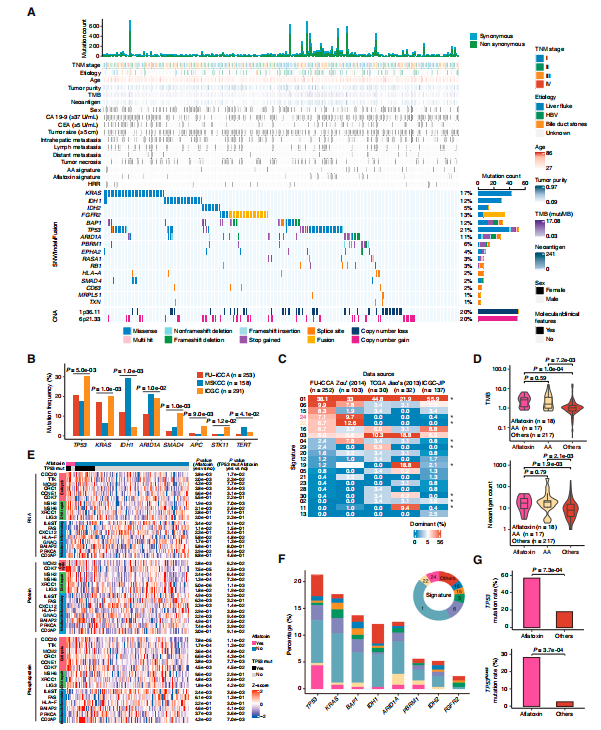
图1 FU-iCCA队列的基因组图谱
作者使用变化最大的1,376种蛋白质进行聚类(图2A),鉴定了4个不同的蛋白质组亚型(S1-S4),这些亚型具有不同的临床、基因组、免疫学和微环境特征。S1展现出丰富的炎症蛋白表现,例如CD14、MPO和C5AR1。S2具有最高水平的癌症相关成纤维细胞和ECM相关的蛋白质,包括FAP、POSTN和FLT1。S3的特点是MAPK和代谢蛋白升高,例如ACAT1、FASN和IDH1。S4保留了粘附和胆道特异性蛋白的最大表达,例如ANXA4、KRT18和EPCAM(图2B)。
临床指标中,S1亚型患者CA19-9、肿瘤坏死和肝内转移水平升高。S2亚型患者有较高的淋巴结转移。S3亚型患者以HBV感染为特征。S4亚型富集了低水平CA19-9和较少转移的患者。四个蛋白质组亚型的总生存期(OS)存在显著差异,S1-S4的中位生存期分别为17.2、25.3、36.7和>60个月(图2C)。多因素Cox分析证实蛋白质组学亚型是独立预后因子。重要的是,对于TNM早期阶段的患者,蛋白质组学亚型同样可以对患者的生存率进行分层(独立于CA19-9和CEA水平)(图2C)。此外,作者发现其蛋白质组学亚型与之前报道的胆管癌分子亚型之间存在相当的重叠。每个亚型显示出反复改变基因的不同图谱(图2D)。KRAS突变在S1中显著富集,同时炎症通路上调。TP53突变在S3中占主导地位,伴随着富集的细胞周期和MAPK信号通路。
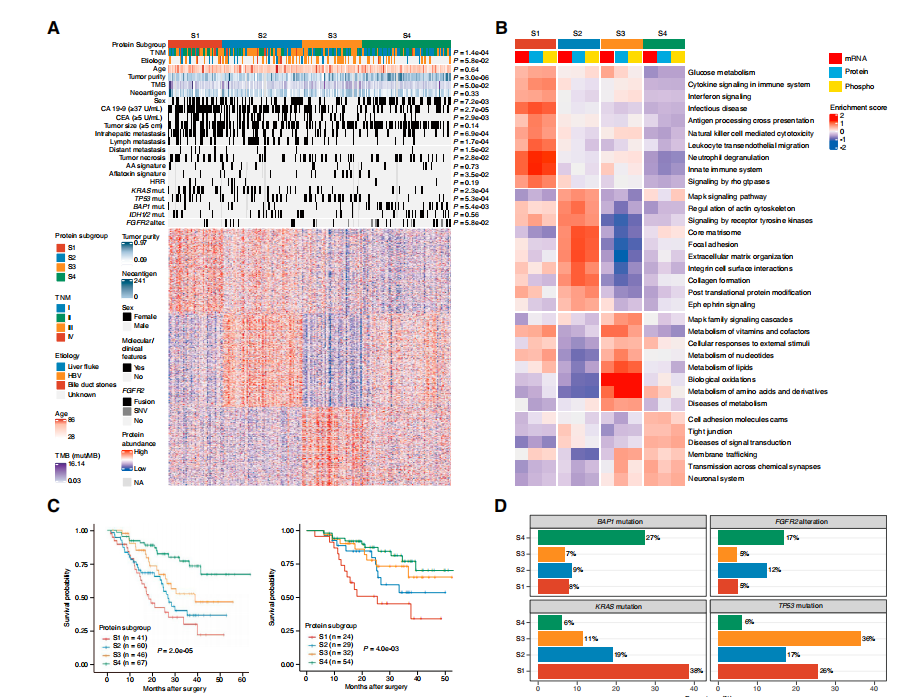
图2 FU-iCCA队列的蛋白质组学分层和相应的分子和通路特征
作者通过监督分析鉴定了19种良好预后相关蛋白质和15种不良预后相关蛋白质(图3A)。其中,HKDC1是最显著的预后正相关蛋白,SLC16A3是最显著的预后负相关蛋白(图3B)。这两种蛋白的丰度在四个蛋白质组亚型中也存在显著差异,SLC16A3在S1中上调,HKDC1在S4中升高(图3C)。在另一个独立的iCCA队列(图3D,n = 222)中,免疫染色结果表明HKDC1低表达和SLC16A3的高表达预示着不良预后,进一步确认了其预后价值。本文数据表明HKDC1可能在iCCA中充当肿瘤抑制因子。实验发现HKDC1的过表达降低了HuCCT1细胞的细胞增殖、集落形成、葡萄糖消耗和糖酵解能力,支持其在iCCA细胞中的抗糖酵解/增殖作用(图3E、3G)。而过表达SLC16A3的HuCCT1细胞表现出更快的增殖和更高的集落形成(图3F),这可能是由于更有效的糖酵解能力(图3H)。SLC16A3敲低显著降低了HuCCT1细胞增殖、集落形成和糖酵解能力。因此,SLC16A3主要通过促进糖酵解代谢在iCCA中发挥致癌因子的作用。
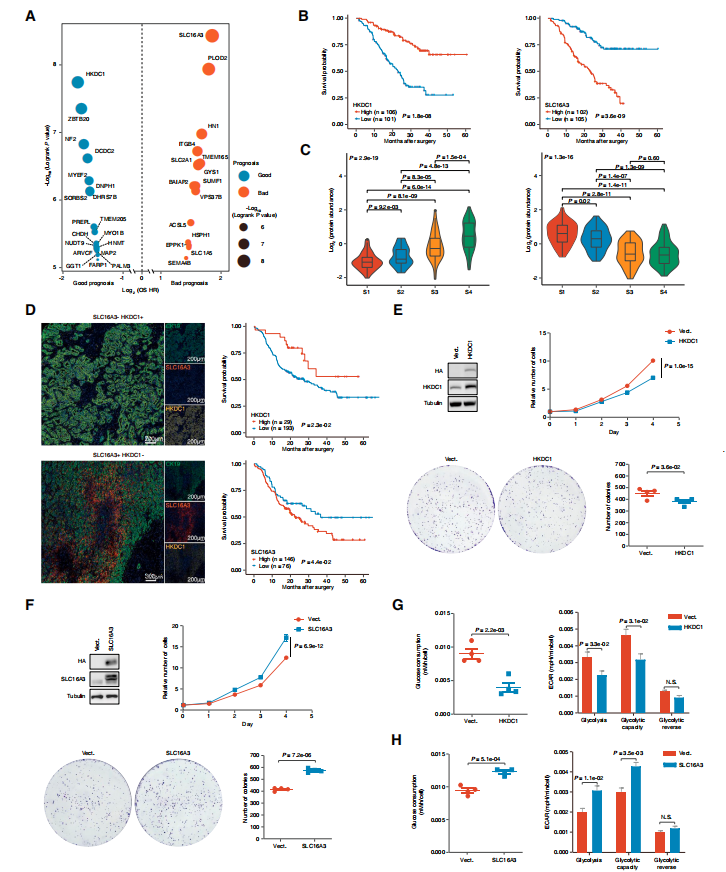
图3 鉴定蛋白质组预后标志物
● 研究结论
基因组学、转录组学、蛋白质组学、磷酸化蛋白质组学等数据的整合分析鉴定了分子机制和疾病亚型,这些信息单独从基因组和转录组是无法完全捕获的。本文数据可能为开发个性化靶向药物和免疫疗法开辟新途径,为深入研究iCCA的致癌、进展和治疗提供宝贵资源。
案例二

中文标题:定量蛋白质组学揭示神经胶质瘤中内吞机制成分的减少的机制
研究对象:人活检胶质瘤组织切片样本
期刊:EBioMedicine
运用技术:非标记定量蛋白质组学
● 研究背景
神经胶质瘤是中枢神经系统中最常见,最具侵袭性的恶性肿瘤。数十年的分子遗传学分析表明,神经胶质瘤积累的遗传改变导致生长因子受体酪氨酸激酶(RTK)和下游信号通路的介质活性增强。其中EGFR、PDGFR、PI3KA和BRAF的功能增强,PTEN和NF1的功能丧失,导致增殖反应加剧。尽管遗传学改变目前已得到充分确立,但关于不同等级和亚类的神经胶质瘤的蛋白质组学变化的信息却很少。为了确定新的靶标和调节机制,本研究采用定量蛋白质组技术分析了从各种神经胶质瘤等级和遗传亚型患者中获取的神经胶质瘤活检样品。
● 研究技术流程
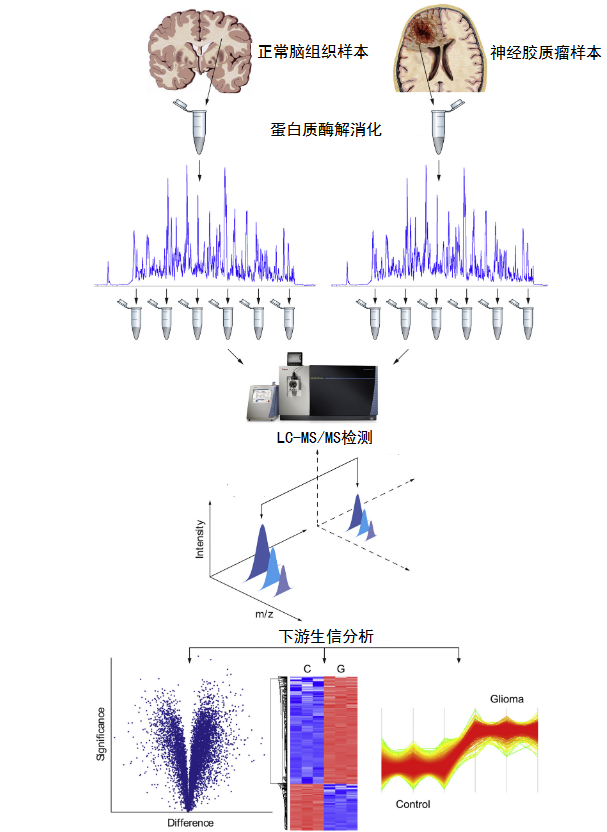
● 研究结果
文章中提到共鉴定出12687个蛋白,其中4029个蛋白质上调,1722个蛋白质下调。挑选2倍倍数变化的差异表达蛋白做功能分析。从下调蛋白质的生物学分类中,研究集中在非常紧密的簇VI上,该簇被注释为“clathrin-结合簇”(图1c)。 对于该簇中存在的蛋白质,计算了单个胶质瘤活检组织和对照组之间的Log2转化率。结果显示,在细胞膜上,参与CCV和CIE载体产生的各个阶段的内吞机制成分显著减少,包括引发剂、主要和替代结构性涂层成分、涂层相关激酶、膜曲率传感器和弯曲器,以及与运输载体的断裂和脱膜有关的因素(图 1d)。具有明确表型的CCV生产中的关键参与者是AP-2,clathrin和dynamin。除了dynamin 2(与dynamin1和3相比,在脑组织中仅少量表达),所有这些成分均显示出蛋白量至少减少了2倍。在分析中,受影响最严重的蛋白是EndoA1-3(图1d)。EndoA1-3是经典CME机制的一部分,目前研究表明其也参与了CIE途径,特别是FEME途径。由于动态蛋白水平降低(CME和多条CIE途径依赖于此),胶质瘤可能在细胞内吞过程中受到损害。
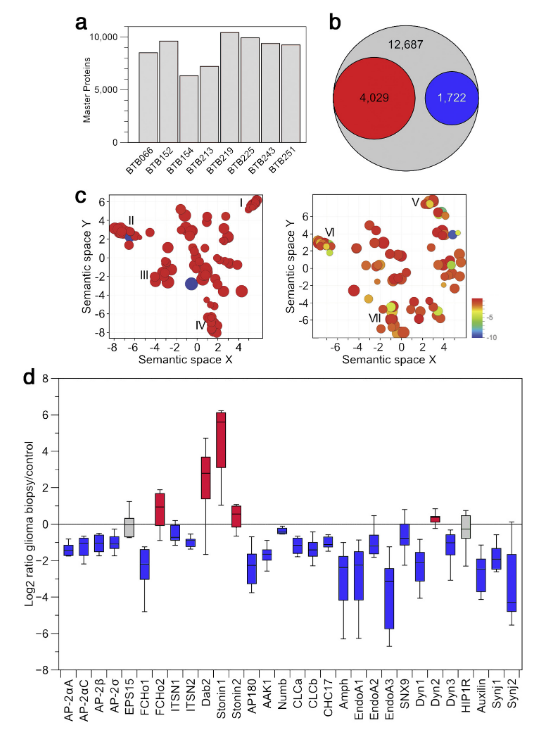
图1 定量蛋白质组学分析显示内吞机制参与成分的强烈减少
为了验证蛋白质组学数据,通过免疫印迹分析了内吞作用不同阶段的一些代表性成分(图2)。AP-2复合物的两个亚单位,这是CME发生和发展的核心成分。主要的脑特异性α-适应素(αA)免疫印迹产生的信号与蛋白质组数据相似,在BTB152、213和219中的表达特别低(图2)。β-亚单位的减少也可以观察到。参与TGN向内皮细胞内转运的AP-1复合物的β1,由于现有的抗体对AP-2的β2不是特异性的,因此其明显较低。AP180在大多数活检中也明显缺失。与蛋白质组数据一致,免疫印迹进一步证明了clathrin重链(CHC17)的大幅减少。CME和大多数CIE新生载流子的分裂是由动力学驱动的。用抗dynamin 1/2的抗体检测胶质瘤匀显示出剧烈下调(图2)。
EndoA1也参与了不依赖clathrin蛋白的FEME途径,在所有分析的活检组织中都被严重消耗掉(图2)。在内质蛋白中,EndoA1是最丰富的,因此可能是大脑中最相关的内质蛋白。以前的研究主要依赖于EndoA2,这是由于使用了非神经元HeLa和BSC1细胞。值得注意的是,EndoA1的下调与许多癌症相关,如乳腺癌、喉癌、肺癌、垂体腺瘤和尿路上皮癌。总之,免疫印迹分析及定量蛋白质组学有力地证实了作者的发现,并提示胶质瘤细胞内吞存在严重缺陷。
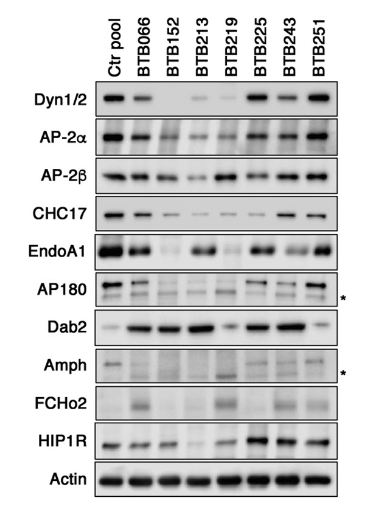
图2 免疫印迹方法分析内吞机制的各成分
● 研究结论
在本研究中,通过定量蛋白质组学分析了不同级别的胶质瘤活检,发现多种内吞机制成分协同减少。通过进一步扩展对其他亚类的分析,发现脑胶质瘤的一个共同特征是细胞内吞的下调。而与细胞内吞有关的个别蛋白质的异常表达与人类癌症有关。研究认为减少内吞机制成分是通过RTKs促进肿瘤发生的策略之一。除了揭示内吞成分的下调,本研究还提供了大量在胶质瘤中定量调节的蛋白质。在胶质瘤研究的背景下,这个数据存储库以及涵盖其他亚型的数据队列对于发现和开发新的治疗策略,以及对于理解其他癌症和一般的致癌具有作用。
参考文献
[1] Dong L, et.al,. Proteogenomic characterization identifies clinically relevant subgroups of intrahepatic cholangiocarcinoma. Cancer Cell. 2022 Jan 10;40(1):70-87.e15. doi: 10.1016/j.ccell.2021.12.006. Epub 2021 Dec 30. PMID: 34971568.
[2] Buser DP, et.al,. Quantitative proteomics reveals reduction of endocytic machinery components in gliomas. EBioMedicine. 2019 Aug;46:32-41. doi: 10.1016/j.ebiom.2019.07.039. Epub 2019 Jul 19. PMID: 31331834; PMCID: PMC6711119.

