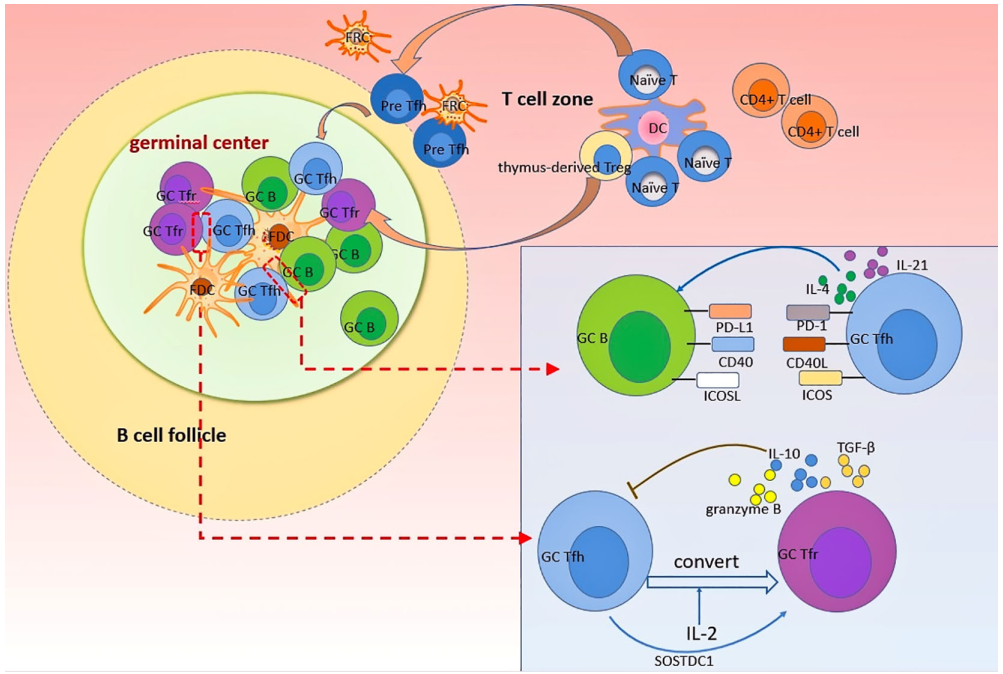
B细胞的活化过程中,会从初级滤泡进入次级滤泡并形成生发中心(GC)这一微结构,在GC中经历突变、亲和力成熟、类别转化后,继续分化为能够产生抗体的浆细胞和记忆B细胞。
在GC中,B细胞的活化受多因素调控,其中的滤泡辅助T细胞(Tfh)是调控B细胞产生抗体的关键,但Tfh细胞数量异常增加会导致自身免疫性疾病,因此同时存在一种抑制性细胞群:滤泡调节T细胞(Tfr)来维持正常免疫耐受。
Tfh/Tfr平衡
Tfh/Tfr细胞平衡对维持免疫耐受非常重要。
Tfh细胞是体液免疫中启动GC反应的CD4+T淋巴细胞,常用功能标志物是CXCR5、BCL6、IL-21。BCL6可以促进CXCR5表达,T细胞依赖CXCR5进入滤泡,而IL-21可以促进CD4+T细胞增殖。
在淋巴滤泡中,B细胞接收滤泡DC细胞(FDC)提呈的抗原后又以抗原肽-MHCⅡ复合物形式继续将抗原递呈给Tfh细胞,Tfh细胞则提供共刺激信号以及细胞因子来活化B细胞。
相反,Tfr充当自身抗体生成的负调节信号,特征是CXCR5+ PD-1+ Foxp3+。
一方面,Tfr以CLTA-4依赖性的方式抑制GC中Tfh、B细胞的增殖和功能;另一方面,Tfr还分泌抗炎细胞因子IL-10、TGF-β、颗粒酶B;而且Tfr还会抑制B细胞代谢途径来减弱B细胞对Tfh信号的反应。
Front Immunol. 2021 Mar 26;12:641013.
Tfh与Tfr的作用截然相反,二者之间的平衡对微调GC反应必不可少,在多种自身免疫性疾病中发生Tfh/Tfr细胞平衡失调。
cTfh/cTfr比例与IgG生成和自身免疫性疾病活动度正相关,二者可能随着GC的变化而改变,可作为体液免疫活性和疾病严重程度的指标。
Tfr的起源和定位
对Tfr的调节是维持Tfh/Tfr平衡的关键,但我们对其起源、发育阶段、组织内生物学功能的认知还不全面。
起初,人们认为Tfr仅仅来自胸腺衍生的Foxp3+Treg细胞,但后续有研究表示Tfh能够以IL-2依赖的方式转化为Tfr,这促进了调控Tfh/Tfr平衡成为治疗自身免疫性疾病的新方向。
此前对于人类的Tfh/Tfr细胞的研究主要限于循环中(cTfh/cTfr),最近研究人员发现人类扁桃体中CD25hi细胞群分为三类:
Treg:CD25hi CXCR5- PD1lo,
Tfr:CD25hi CXCR5+ PD1+,表达比Treg更高水平的Foxp3,可抑制反应性T淋巴细胞(Tresp)增殖;
Tfh:CD25hi CXCR5+ PD1hi,可以分泌IL-10,但没有抑制Tesp细胞的功能。
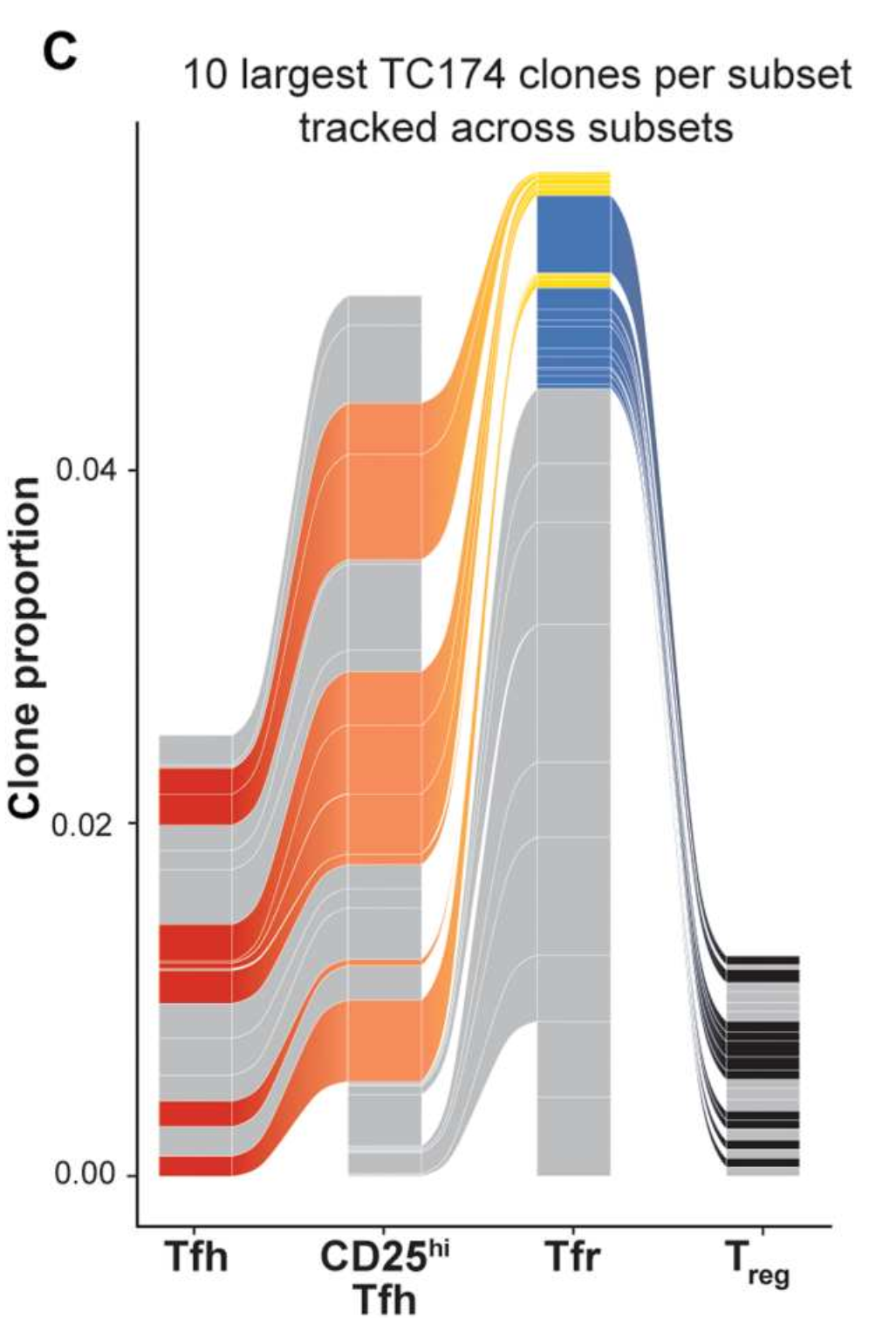
Tfh常规被认为是CD25-CXCR5-PD1+,于是通过对这三类细胞进行了单细胞分析,发现Tfr——CD25hi Tfh间存在共享的克隆谱系,但与Tfr——Treg间共享克隆谱系并不重叠。
Sci Immunol. 2023 Apr 14;8(82):eade8162.
使用重组IL-2后,发现CD25hi Tfh第5天开始表达Foxp3,并可以抑制Tresp细胞,这类亚群便是以IL-2依赖方式分化为Tfr的关键。这也证实了Tfr可来自不同细胞群。
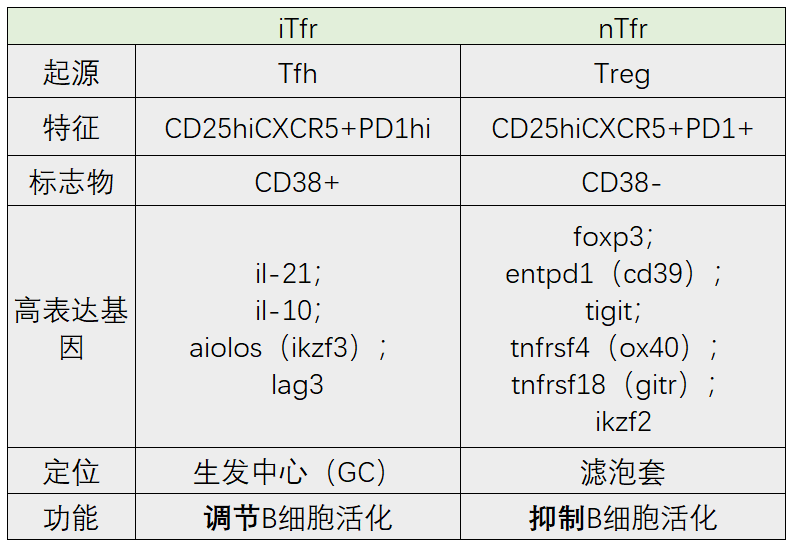
按照克隆关系,将Tfh来源定义为iTfr,Treg来源定义为nTfr。
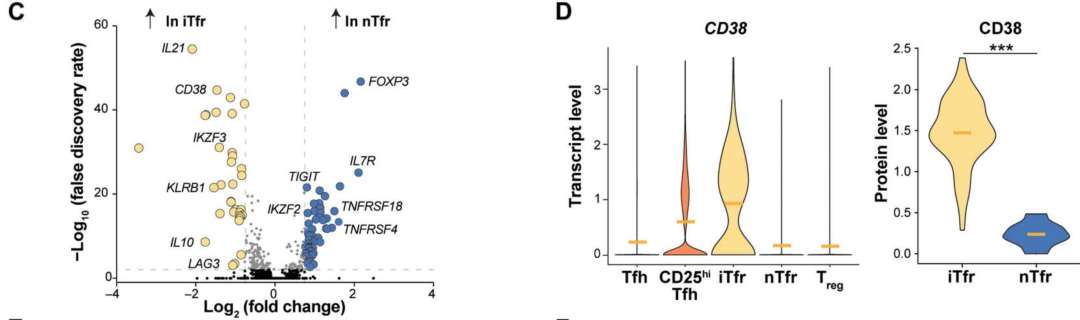
通过转录分析,发现nTfr和iTfr拥有86个差异表达的基因,各自有不同的高表达基因:
iTfr:il-21、il-10、aiolos(ikzf3)、lag3。
nTfr:foxp3、entpd1(cd39)、tigit、tnfrsf4(ox40)、tnfrsf18(gitr)、ikzf2。
其中CD38表达差异最明显,也被用作区分两类细胞的标志物。
Sci Immunol. 2023 Apr 14;8(82):eade8162.
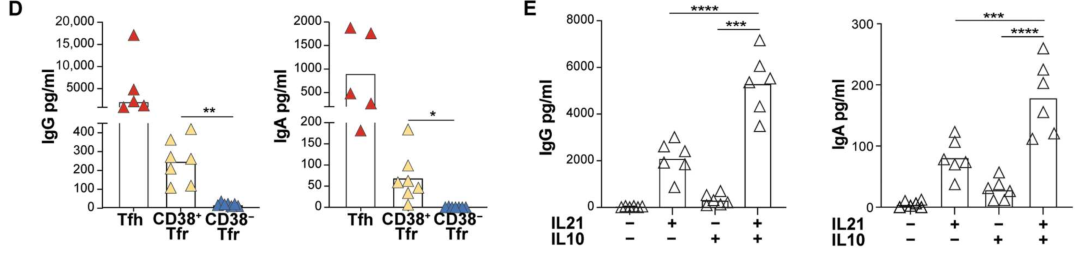
iTfr(CD38+)分泌IL-21的能力比nTfr(CD38-)高2.7倍,能够促进共培养的GC B细胞产生更多的IgA。
但iTfr(CD38+)细胞可以受IL-10和IL-21分泌的调节,而对B细胞活化产生不同的影响,因此将iTfr(CD38+)定义为调节Tfr,nTfr(CD38-)为主要抑制Tfr。
Sci Immunol. 2023 Apr 14;8(82):eade8162.
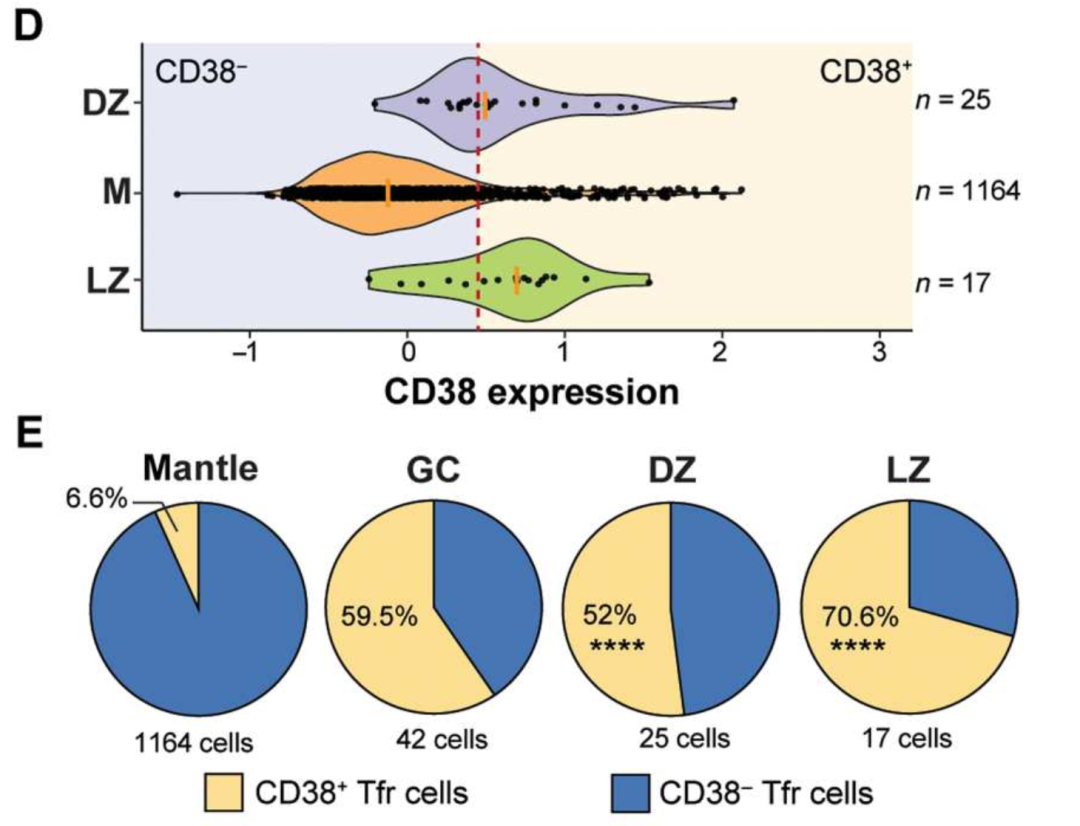
通过染色成像,发现iTfr(CD38+)定位于GC内,CD38-Tfr定位于滤泡套内(大多数)。
DZ:暗区,LZ:亮区
Sci Immunol. 2023 Apr 14;8(82):eade8162.
不同来源使Tfr功能多样化:
位于GC中的iTfr具有抑制功能,并在一定程度上帮助B细胞活化;
而位于滤泡套内的nTfr则是纯粹的抑制细胞。
小结
B细胞在活化为浆细胞或记忆B细胞的过程中,在次级淋巴滤泡中移动的方向为暗区→明区→滤泡套,滤泡套中的nTfr则是控制活化程度的关键。
在GC中,暗区的B细胞经历增殖后进入明区,与Tfh细胞进行信息交流进行活化,但若是接收到的Tfh刺激信号较弱则会重回暗区,iTfr可能在此处参与B细胞活化的初步调控。
对于Tfr的研究不仅可以进一步理解自身免疫性疾病的发生机制,对其来源和定位也为调控免疫活性提供了一定的参考价值。