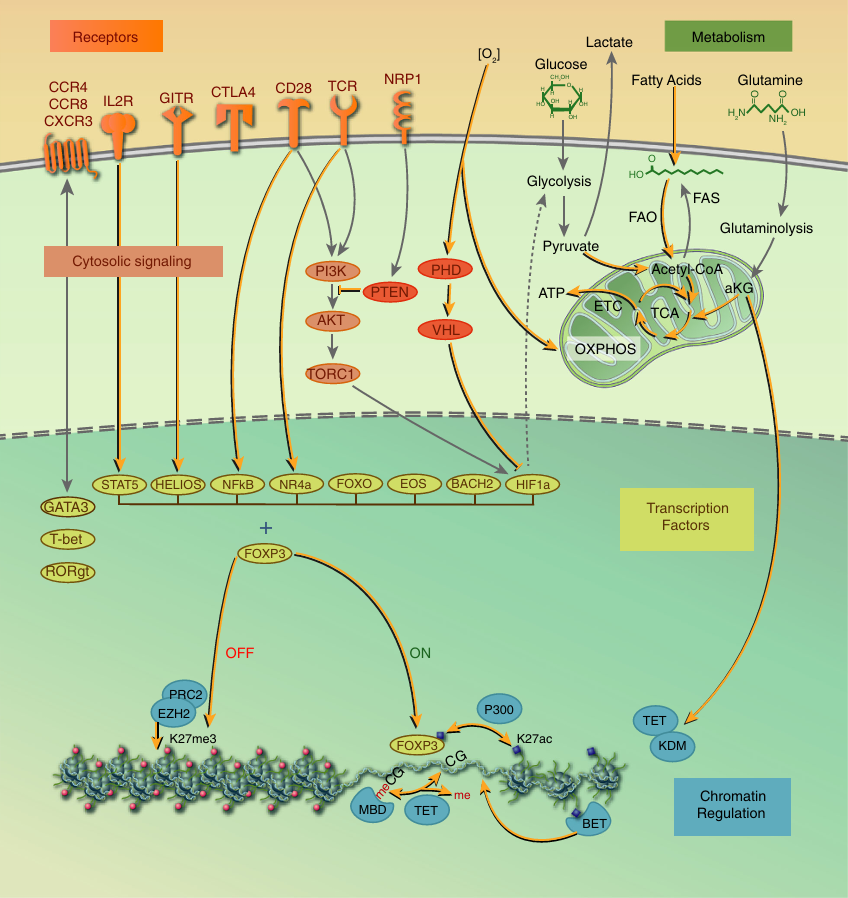
Treg 细胞的功能调节涉及多种激酶,这些激酶通过调控细胞代谢、转录、表观遗传及信号转导等途径,精准控制 Treg 细胞的发育、存活、增殖和免疫抑制能力。
一、AMPK
核心作用
代谢稳态调控
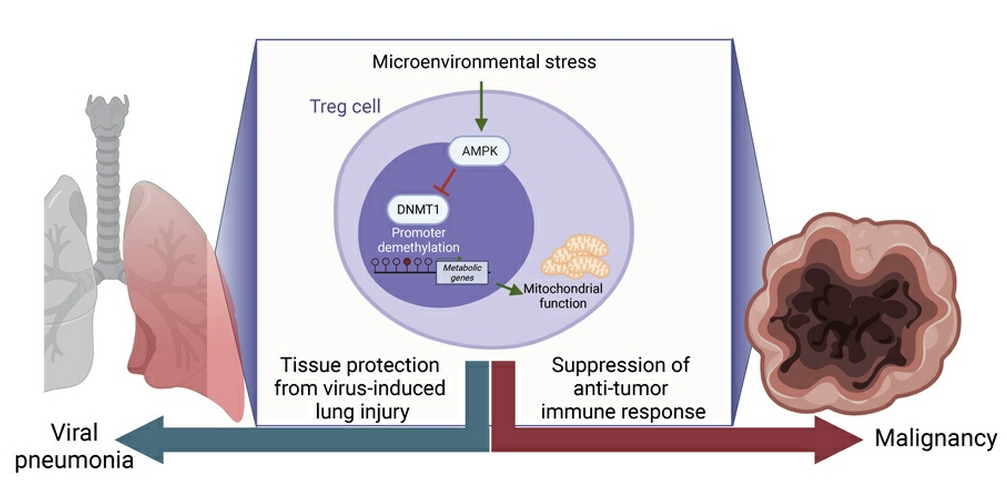
作为能量传感器,AMPK 在 ATP 不足(如肿瘤微环境的葡萄糖匮乏)时被激活,通过促进线粒体氧化磷酸化(OXPHOS)维持 Treg 细胞的代谢适应。
表观遗传调控
磷酸化 DNA 甲基转移酶 1(DNMT1),抑制其活性,从而降低代谢基因(如 Ppargc1a、线粒体电子传递链基因)启动子的甲基化水平,促进转录激活。
缺失 AMPK 会导致 Treg 细胞线粒体质量下降、有氧呼吸受损,在肿瘤和病毒性肺炎模型中表现为免疫抑制功能减弱。
实验证据
在 Treg 特异性 AMPKα1/α2 双敲除小鼠中,B16 黑色素瘤生长受抑,瘤内 CD8⁺ T 细胞活化增强;流感病毒感染后肺损伤加重,死亡率升高,提示 AMPK 是 Treg 适应代谢应激的关键。
二、mTOR
核心作用
代谢开关调控
mTORC1 通路激活促进糖酵解和合成代谢,抑制线粒体氧化磷酸化,而 Treg 细胞的抑制功能依赖低 mTOR 活性和 OXPHOS。
雷帕霉素(mTOR 抑制剂)可增强 Treg 细胞稳定性,促进其在自身免疫病中的保护作用。
转录与功能维持
过度激活 mTOR 会导致 FOXP3 表达不稳定,诱导 Treg 细胞向促炎表型(如 Th1/Th17)转化,丧失免疫抑制能力。
实验证据
Treg 特异性 mTOR 缺失小鼠表现出更强的免疫抑制功能,可缓解实验性自身免疫性脑脊髓炎(EAE);反之,mTOR 激活剂(如 IGF-1)会削弱 Treg 细胞功能。
三、Akt
核心作用
生存与增殖调控
Akt 通过 PI3K-Akt 通路传递生长因子(如 IL-2)信号,促进 Treg 细胞存活和增殖。
代谢重编程
激活 Akt 会增强糖酵解,但过度激活可能抑制线粒体代谢,损害 Treg 细胞功能。
与 FOXP3 互作
Akt 磷酸化 FOXP3,调节其核定位和稳定性,影响 Treg 细胞的抑制能力。
doi:10.1111/imm.13058
实验证据
敲低 Treg 细胞中的 Akt 会导致细胞凋亡增加,而持续激活 Akt 则诱导 Treg 细胞向效应 T 细胞转化,引发自身免疫症状。
四、GSK-3β
核心作用
转录因子调控
磷酸化 FOXP3,促进其降解,抑制 Treg 细胞发育和功能。
抑制 GSK-3β(如通过锂剂)可稳定 FOXP3,增强 Treg 细胞的免疫抑制能力。
代谢与炎症调控
GSK-3β 通过调控糖代谢和炎症因子(如 NF-κB 通路)间接影响 Treg 细胞功能。
实验证据
在小鼠模型中,GSK-3β 抑制剂可增加 Treg 细胞比例,缓解结肠炎和哮喘等炎症性疾病。
五、CDK
核心作用
细胞周期调控
CDK4/6 驱动 Treg 细胞增殖,其抑制剂(如 palbociclib)可阻滞 Treg 细胞于 G1 期,减少其在肿瘤微环境中的浸润,增强抗肿瘤免疫。
功能可塑性
CDK2 通过磷酸化 FOXP3 调控其稳定性,影响 Treg 细胞在炎症和肿瘤中的功能切换。
实验证据
阻断 CDK4/6 可减少小鼠肿瘤中 Treg 细胞数量,增强 PD-1 抑制剂的抗肿瘤效果。
六、其他关键激酶
LKB1
作为 AMPK 的上游激酶,通过激活 AMPK 维持 Treg 细胞线粒体代谢和功能稳定性。LKB1 缺失会导致 Treg 细胞线粒体功能缺陷,引发自身免疫病。
PKCθ(蛋白激酶 Cθ)
在效应 T 细胞中促进免疫应答,但在 Treg 细胞中通过调控细胞骨架和迁移能力,影响其向炎症部位的募集。
临床转化方向
肿瘤治疗
抑制 AMPK 或激活 mTOR 可削弱肿瘤微环境中 Treg 细胞的免疫抑制功能,增强免疫治疗效果。
自身免疫病
激活 AMPK 或抑制 GSK-3β 可稳定 FOXP3,增强 Treg 细胞的抗炎能力(如二甲双胍、锂剂的潜在应用)。
联合策略
靶向激酶与表观遗传调节剂(如 DNMT 抑制剂)联用,可能更精准调控 Treg 细胞功能。
这些激酶不仅是 Treg 细胞生物学的关键机制靶点,也为多种疾病的免疫干预提供了潜在药物开发方向。
参考资料
AMPK is necessary for Treg functional adaptation to microenvironmental stress during malignancy and viral pneumonia,J Clin Invest. 2025;135(9):e179572. https://doi.org/10.1172/JCI179572
Phosphoinositide 3-kinase d is a regulatory T-cell target in cancer immunotherapy,Immunology, 157, 210–218,doi:10.1111/imm.13082