全长一小时 · 深度学术对话

特邀嘉宾
Hans Clevers 教授
现任职位Hubrecht研究所PI;乌得勒支大学分子遗传学教授;Princess Máxima Center 类器官研究团队客座科学家
学术造诣首次发现成体干细胞标记物 LGR5;确立 Wnt 通路核心机制;开创成体干细胞来源的类器官(Organoids)培养技术。作为类器官技术开创者以及Wnt信号通路研究领军人物,学术产出极其丰厚,在Cell、Nature及Science三大顶级期刊上发表超60篇高水平研究论文,总引用次数已突破310,525次(近五年贡献约12.7万次),h指数(h-index)263,i10指数805。
特邀嘉宾
林琳 博士
现任职位中国科学院上海生化细胞所研究员、博士生导师。
学术背景Hubrecht研究所 Clevers 实验室博士后 (2020–2024),专注于成体干细胞来源的类器官研究,以第一/共通讯作者在Science、Cell Stem Cell等期刊发表多篇研究论文。
参与者名单:
Juliana Amorim / Bruno Matuck (主持人) · Henry Weith / Yvonne Lin (提问主持) · Hans Clevers / 林琳 (嘉宾)
2026年开年,Exocrine Gland Biology Podcast 迎来重磅嘉宾——类器官技术的奠基人 Hans Clevers 教授。作为 Wnt 通路研究的领军人物,Clevers 教授以超 31 万次的学术引用和 263 的 h 指数,深刻改写干细胞生物学版图。
与他同台对谈的是其实验室博后、现任中国科学院上海生化细胞所研究员的林琳博士。两人围绕近期发表于 Cell Stem Cell 的黏膜下腺(SMG)类器官研究,从免疫学的渊源谈到未来药物研发的伦理转向,为青年学者奉献一场跨越代际的深度学术思辨。
核心洞察 / KEY INSIGHTS
01
范式转移:从 LGR5 到全器官模拟
Hans Clevers 回顾了如何从 T 细胞免疫学意外撞入 Wnt 领域,并详述了 2009 年首个“微型肠道”诞生的冒险历程。
02
还原论美学:简洁即是力量
林琳提出可在肠道类器官中整合多种细胞进行复杂共培养,但认为该体系可能过于依赖单细胞测序且难以解析。Hans Clevers则强调其团队坚持“简化还原”策略,通过精确添加关键因子而非直接引入混合细胞,以确保实验可控、结果清晰,从而在机制层面高效推进研究。
03
产业重塑:非动物性替代法的崛起
分析 FDA 强硬立场下类器官的标准化趋势,以及中国在自动化培养平台领域的独特工程机遇。
04
科学家精神:进入“黑暗地带”的勇气
Hans 寄语青年 PI:信任同事、保持透明、勇于进入竞争对手尚未涉足的未知领域。
01
追本溯源:从免疫学到Wnt通路的转向
Juliana:大家好,我是Juliana,欢迎回到“外分泌腺生物学(Exocrine Gland Biology)”播客。这是由外分泌腺生物学小组发起的项目。很高兴与大家一起进入第二季第4期。本季我们致力于让资深与青年研究者同场交流科学。这期节目很荣幸邀请到两位嘉宾。林琳博士,她在Hubrecht研究所完成了博士后训练,近期在中国科学院上海生化细胞所组建了自己的课题组;以及Hans Clevers教授,他是乌特勒支大学分子遗传学教授,同时也是Princess Máxima Center类器官研究团队的客座科学家,同时担任罗氏(Roche)制药研究与早期发展(pRED)与人类生物学研究所(IHB)负责人。Clevers 教授职业生涯中获奖众多,并在顶级期刊发表大量论文。
Bruno:今天我们聚焦他们合作的论文《Human airway submucosal gland organoids to study respiratory inflammation and infection》,近期发表于 Cell Stem Cell。两位能否先自我介绍,并简要概述这项研究的核心目标?
Hans Clevers
也许我先来,通常应当“女士优先”。昨天我在荷兰乌得勒支大学做了一个讲座,主持人介绍时让我意识到,我在乌得勒支读大学已经是50年前的事了。后来我去了波士顿,在哈佛学习分子生物学(那是上世纪80年代),然后把这些带回荷兰。我最初研究的是免疫学,在自己的实验室里想要找到 T 细胞特异的转录因子,解释 T 细胞如何从骨髓分化而来。因此, 我们克隆了 TCF(T-cell factors),后来发现它们其实也是 Wnt 信号通路的关键组成。于是我和我的实验室逐渐从 T 细胞免疫学转向了发育生物学,因为当时 Wnt 主要在果蝇、线虫和爪蟾等模型中被研究。那时候我还是临床免疫科主任,但系主任觉得医院不是做这类研究的好地方。于是在大约2002年,我们就搬到了 Juliana 刚提到的 Hubrecht 研究所,也就是Lin开展博后研究的地方。
02
干细胞革命:LGR5与“Mini-Gut”的诞生
Hans Clevers
与此同时,我们发现 Wnt 通路不仅在发育中重要,它对成年个体的干细胞维持也非常关键,尤其在肠道。我们当时聚焦于此。我们和Bert Vogelstein 也发现 Wnt 通路突变会导致结直肠癌。所以我们知道 Wnt 对肠干细胞非常关键,尽管当时肠干细胞还未被正式发现,但它们是哺乳动物体内最活跃的干细胞。如果激活 Wnt 通路,就会形成结肠癌。我们双线并行地研究,两年后(2007年前后),来自英国、后来在新加坡任教的博士后 Nick Barker 找到了一个标记——LGR5,在Lieberkühn隐窝底部标记肠上皮中极小的一群细胞。Nick 证明这些 LGR5 阳性细胞就是肠上皮的干细胞。后来他又发现,LGR5 也标记许多其他组织的干细胞,可能几乎涵盖所有上皮组织的干细胞类型。
又过了两年,2009 年,Toshi Sato 开始尝试培养这些干细胞。当时这是不小的冒险,因为大家普遍认为正常细胞是培养不起来的。我试图劝几位博士后接手,但没人愿意,担心“三年白干、断送学术生涯”。但Toshi 接受了挑战。当时我们对肠道上皮隐窝中维持干细胞高度活跃的生长因子条件已有相当了解,例如表皮生长因子以及Wnt信号。我们知道还需要抑制BMP。我们采用3D培养——这是Mina Bissell的建议,她率先将基质胶用于上皮细胞的3D培养。出乎意料的是,我们本想获取单个干细胞并大量扩增肠道干细胞,却得到了这些非常有秩序的结构。Toshi 很快意识到,这些结构像它们来源组织——肠上皮的“复制品”,包含肠上皮所有细胞类型,形态也相似。他称之为“mini-gut”。更意外的是,它们可以无限传代培养,还能移植并形成正常组织,不是肿瘤。细胞系移植总会成瘤,但类器官生成的是正常组织。随后 CRISPR 出现了,借助它我们几乎可以在类器官里实现任何遗传改造,Lin稍后可能会详细说明。
由于LGR5干细胞不仅存在于肠道,许多其他器官也有LGR5标记的干细胞,我们逐步尝试,通过稍作调整(通常是让培养条件更复杂一些),成功培养了其他器官的类器官,例如胃上皮(我想这是第一个),此外还有肝、胰腺、前列腺、乳腺。甚至蛇的毒腺,实际上是爬行动物的毒腺,也能以类器官形式培养。因此,实验室过去十五年的模式基本上是:每当有新的博士后或博士生加入,我们会探讨哪些组织尚未研究,然后寻找能提供该组织的临床科室,与那里的临床医生或科学家展开紧密合作。我想林琳接手了其中几个项目,其中之一就是气管黏膜下腺体——在Lin向我展示她的项目成果之前,我甚至从未听说过这个腺体(笑)。
简而言之,我认为这种方法非常成功,我们的研究方式极具机会主义色彩。我们曾是免疫学家、发育生物学家、癌症生物学家、肠道生物学家,而现在我们几乎是研究任何器官的生物学家。典型的工作模式是:你需要勇气,需要为新项目带来独特视角,而我们目前始终带着类器官技术。我们擅长创建类器官,但对所研究组织的了解可能不深,因此需要寻找优秀的合作者,他们会告诉我们“这个方向很重要,这个问题我们可以共同解决”。这种模式效果很好。Lin会为我们讲述一个很好的例子。
林琳
正如 Hans 提到的,2020年至2024年间,我在他的指导下进行博士后研究。类器官工作深刻塑造了我对人类组织生物学的思考方式,即在体外培养成体干细胞来源的类器官。其目标是建立一个高度动态的实验系统,以捕捉成体组织中全部的细胞异质性。同时,这个系统也具有很强的可控性:你可以改变组织环境,让其暴露于不同的细胞因子或微环境因子中,并追踪其变化。它还是一个出色的可示踪系统,例如可以通过报告基因标记特定细胞类型来追踪细胞身份。此外,这也是一个极佳的人类生物学研究系统,因为它能在体外最大程度地模拟人类生物学。
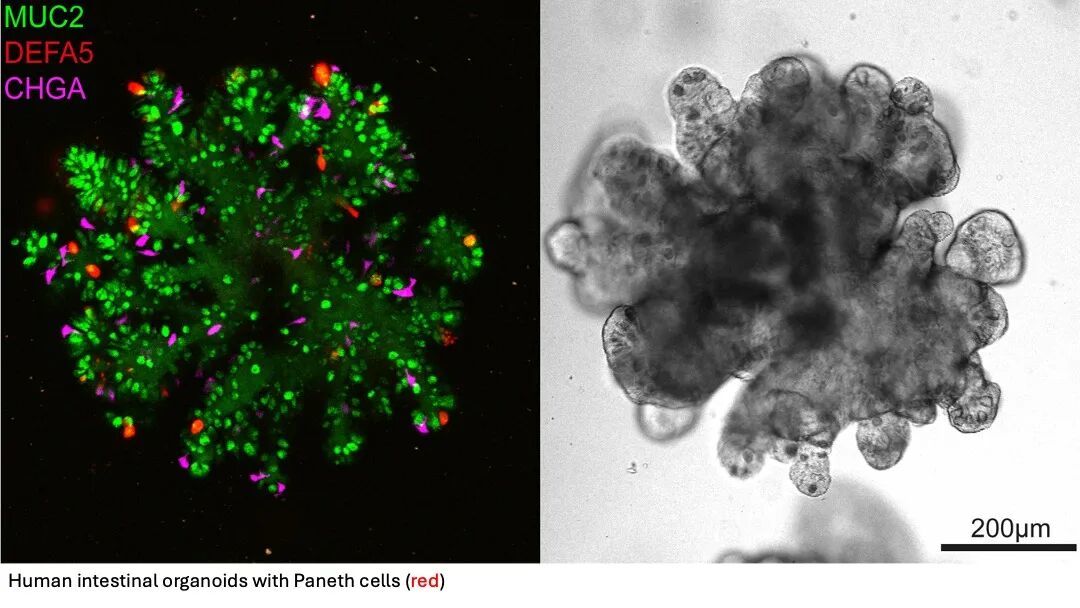
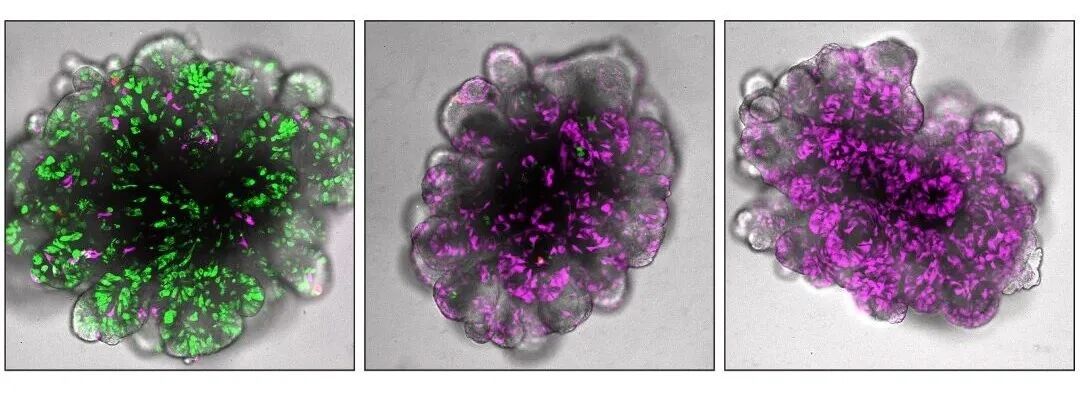
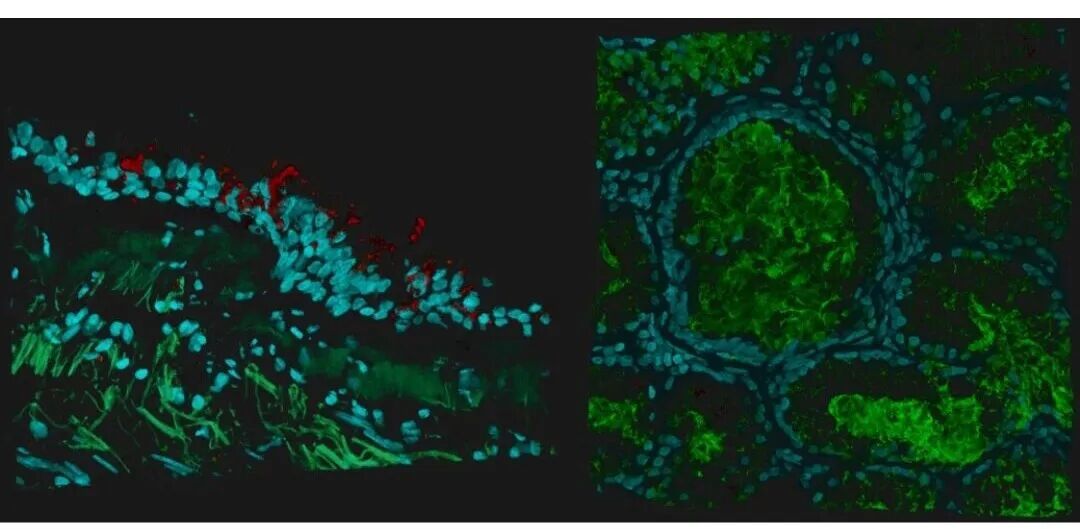
我加入 Clevers 实验室后,除了这项黏膜下腺类器官工作,我最初还研究肠道类器官。我曾尝试优化人肠道类器官培养体系,在该项目中我们发现细胞因子IL-22可以诱导肠道类器官中潘氏细胞的分化。由于我此前具有CRISPR技术的研究背景,我随后利用类器官系统进行了CRISPR筛选,找到了调控肠道类器官细胞命运决定的转录因子。至于这篇黏膜下腺类器官的论文,我觉得它很有意思。因为正如Hans所说的,我们试图探索实验室从未涉足的领域。我查阅文献后发现,黏膜下腺体是人类气道上皮中一类非常重要的特化分泌腺,具有关键功能。但人们通常更关注肺泡、肺部生物学,气道生物学相对“不热门”。因此我认为,这会是一个学习新知识、在实验室开启新项目的好机会。这就是我最终选择研究黏膜下腺体的缘由。
Hans Clevers
我想补充一点:Lin提到她在做黏膜下腺体研究之前,她曾利用白细胞介素22尝试改善肠道类器官。事实上,IL-22 曾被顶级期刊报道为干细胞和上皮增殖的驱动因子。但我们对此一直有怀疑。我们非常漂亮地证明了:IL-22 并不会促进干细胞增殖。实际上,它并不驱动干细胞,而是诱导形成大量漂亮的 Paneth 细胞(肠上皮中特殊的一类具有免疫功能的细胞类型)。而且事实上,有不少药企正在把 IL-22 作为炎症性肠病(IBD)的潜在治疗靶点。而Lin的研究提示这可能并不会起到预期效果,因为它主要改变分化,而没有帮助干细胞层面的修复。我们可能在无意中“毁掉”了一些制药公司的项目。
03
病因探寻:慢性疾病建模的挑战与纤维化
Yvonne:谈到肺相关疾病,很多人对气道类器官也很感兴趣,比如 COPD、衰老、纤维化等慢性疾病,它们对黏膜下腺的负担很重。你们认为当前或未来的类器官系统能否复现这些很难在体内建模的长期慢性病程?是否已有策略可以模拟这些疾病的某些阶段?
林琳
像 COPD、衰老、纤维化这类慢性疾病,即使用小鼠模型也很难真正模拟,因为其生理结构和病理过程与人本身就有差异。我们可能需要用不同方式来实现“慢性化”的类器官建模。一种思路是做反复的损伤—修复循环,或者长期施加某种炎症性/损伤性生态位刺激,让干细胞在长期环境压力下逐步改变行为,从而更接近慢性病过程。另一种思路是直接“工程化”细胞的年龄状态,不过这会更复杂,比如通过端粒相关的操控,或用表观遗传编辑把细胞推向更“衰老样”的状态,然后再尝试用类器官去捕捉那些晚发疾病的特征。
Hans Clevers
我再补两点。一个是炎症性肠病(IBD)。我们在儿童医院的合作者发现,从克罗恩病或结肠炎病变部位建立的类器官,在最初几代会呈现严重炎症状态,但培养一段时间后恢复正常。这意味着炎症性肠病并非上皮细胞本身的原发性缺陷,而是微生物组或免疫系统持续攻击上皮细胞,导致干细胞过度代偿。一旦将干细胞置于适宜的类器官环境中后,炎症信号消失。这提示慢性炎症疾病(如COPD或哮喘)的建模挑战在于病因不明。我们观察到白细胞介素水平波动导致组织损伤与再生,但不知根本病因。在缺乏病因认知的情况下,我们只能模拟症状而非疾病本质——动物模型也是如此。这是一个长期存在的挑战。我在罗氏工作的这些年也深刻体会到,无论是COPD、IBD、系统性红斑狼疮还是多发性硬化症等慢性炎症疾病,用现有模型研究时,由于模型并非由真实病因驱动,我们永远无法找到根治方法,只能获得对症治疗方案。这或许是动物模型极难甚至无法破解的困局,也正是类器官领域需要突破的方向——很可能必须引入真正的罪魁祸首(比如调节性T细胞或特定微生物组),构建出能重现疾病初始过程的环境。
另外,我还有个“执着”的观点。纤维化是任何慢性损伤器官的必然结局。无论是肺、肝、胰腺还是肠道,只要长期受损就会发生纤维化。我坚信单纯抑制纤维化对患者并无帮助,因为干预时机已经太晚。本质上,纤维化是一种保护性反应,是器官为维持结构完整而形成的疤痕组织。就像心肌梗死后,心肌细胞无法再生,心脏只能通过纤维化疤痕来替代缺损部位。如果此时阻止心脏纤维化,反而会导致心脏破裂危及生命。因此对于肝纤维化和特发性肺纤维化,我认为数十年来抑制纤维化的治疗尝试方向有误。纤维化本身不是治疗靶点,它只是机体应对损伤的反应。我们真正需要追寻的是病因——而这往往仍是未知数。
04
工程与简洁:类器官研究的哲学争论
Henry:在构建更复杂系统、增强细胞间通讯方面,如果像你们论文最后一幅图那样“分选单个细胞再共培养”,是否会缺少微环境,比如基质细胞?能否做“类器官-类器官”的共培养,或在体外重建类似 TME 的多细胞微环境?可行性如何?
林琳
在肠道类器官方面,已经有论文发表过:你可以把不同的组成部分放在一起,比如你说的成纤维细胞、上皮细胞、免疫细胞,甚至可以用同一位供体来源的自体 T 细胞,把它们组合到一起做共培养。对我来说,我觉得那样还是太复杂了,因为你的读出方式往往会变成单细胞 RNA 测序,而这可能几乎是你唯一可用的读出。我认为现阶段更合理的方式可能是:一个一个来,一层一层来,每次只加一层复杂度。并且读出应该是更可控、更可追踪的。你需要一个很好的(评估体系),也就是说,除了单细胞测序之外,你还应该有其他方式来解答生物学问题。
Hans Clevers
(笑)这个回答显示出你在我实验室多年。我认为类器官的优势在于其简洁性。这是一种非常还原论(reductionist)的系统。但只要你哪怕增加一种额外的细胞类型,你需要做的对照数量就会急剧上升。所以你并不是第一个问我这个问题的人,已经有成千上万的人问过我,比如在“基质细胞—肿瘤细胞”这个话题上大家也总这么说:基质细胞对癌症太重要了。对此我通常会反驳。当你把基质细胞加进去的时候,如果你并不清楚自己到底加了什么,那么每一份基质样本都会不同。而我们实际上是把“基质细胞的作用”替换成了它们产生的关键因子,并且我们用一种极其可控的方式来做——你能精确知道加入了多少 EGF、多少 WNT 等等。所以这是一种研究风格,而且事实证明它也非常有效。所以我们基本上专注于最核心、最简单的相互作用。比如你谈的是两个细胞类型之间的互动,我们就尽量把系统简化到能看出一些“基本规律”。这样通常会得到非常“黑白分明”的结果。当你观察到的确实是一个真实现象时,通常你每次做实验都会非常强烈地看到它。这样你就能快速推进并做出发现。然后我们再回到真实情境,去检验我们在简化系统中总结出的规律,在更复杂、疾病相关的系统里是否仍然成立。很多其他实验室,往往借助工程技术,填补简单体系与复杂生理间的鸿沟。但正如Lin刚才说的,现有技术要做到这一点非常困难。因为你需要为你加进去的每一个变量做大量对照,一次实验可能就需要无数个孔板。所以我认为,仍然有足够多的问题可以用非常简单的系统来回答。也正因为如此,我通常会尽量劝我的实验室成员不要过度增加复杂性。当然,也有些实验室正好相反,这就是一种研究风格的差异。
Yvonne:关于“可控与简洁”的思路,另一个争论是标准化:大家做类器官的方法太多,如何建立跨实验室的一致性?两位怎么看哪些步骤对标准化至关重要?
林琳
我想先给一个比较“天真”的看法,之后 Hans 会补充更深入的观点。我认为类器官领域仍然很年轻。每年都有很多不同实验室发表新的培养方案,并展示他们的体系可以产生更成熟的细胞类型。比如肝类器官,今年就有两篇非常好的论文发表在成年肝细胞类器官方向上。但如果谈到“如何标准化培养方式”,我觉得最重要的其实是先标准化“如何评价类器官”。而且这种评价必须是组织特异性的。举例来说,对肠道类器官,你怎样判断它是一个“好的”肠道类器官?它是否具有足够的细胞异质性?包含哪些细胞类型?它是否能体现取材区域的特异性(也就是活检来自哪个肠段、它是否保留了该区域的特征)?所以我认为,现在就去讨论“统一培养方法”可能还太早,更现实的是先把评价体系做统一、说清楚。
Hans Clevers
从我这些年在产业界的经验来说,产业界对类器官、尤其是 3D 类器官的采用一直比较慢,原因很多:它很复杂,需要很高的操作技能,成本高,而且重复性不够好。因此,如果我们希望类器官在药物研发或者诊断中发挥作用,就必须要有标准化的培养流程、标准化的读出方式,甚至需要自动化的类器官培养系统。同时它必须更便宜、更简单、更稳健。对产业应用来说,这种标准化尤其关键——包括一个最基本的问题:什么情况下我们可以把某个体系称为“类器官”(定义要清晰)。另外我也想说,和我们使用的成年组织干细胞相比,iPS(诱导多能干细胞)领域在结果上更不可测些。成年干细胞其实“很固执”(pretty dumb),它们来自某个器官,就非常清楚自己要做什么。比如黏膜下腺体类器官永远不可能变成肝类器官,除非你去敲掉一些关键转录因子之类的。因此,成年干细胞没有“随意变成别的器官”的问题;它们通常比较成熟,也很稳定,可以持续培养,在某种意义上几乎像一个细胞系一样稳定。不过即便如此,不同培养条件仍然会影响你得到哪些细胞类型、或者能读出更多什么信息。所以我完全同意需要标准化,尤其是面向工业应用时更是关键。现在也已经有不少相关工作在推进。而且我想,鉴于 FDA 现在已经采取了非常强硬的立场,要求我们在所谓的非动物性替代方法上投入更多。那其中也包括 AI 驱动的模型、计算机(in silico)模型、器官芯片(organ-on-chip)、类器官等等。在这些方向里,一个关键的发展点就是:任何可能被采用的类器官体系都必须实现标准化。
05
全球趋势:中国机遇与减少动物实验
Bruno:英国、美国等国家都在推进减少动物实验。你们是否明显感觉到,越来越多人因为这类政策性趋势而向你们实验室寻求博士后或博士机会?
Hans Clevers
可以说,我的博士后们找岗位从来都不困难,别人也常来问“你还有没有人推荐”。而且我们的团队非常国际化,最近来自中国的成员也很多。我必须说中国对类器官技术的接受度极高,中国在工程方面很强,我相信会在类器官自动化上发挥重要作用。以我在罗氏看到的情况为例(甚至早于我加入之前):药理、毒理、剂量与代谢的制药科学部门已经开始投资体外人源模型。随着 FDA 的推动,我们与药理同事关于“类器官的潜力与需求”的讨论非常活跃。大型公司和 CRO 也越来越感兴趣,纷纷搭建自己的类器官平台,用以替代或补充动物实验。我认为整个药物开发行业都意识到这件事应当发生。尽管很多应用的具体测定(assay)尚未成熟,也不清楚要怎样把它们变为标准化测定,但在 FDA 的推动下,未来几年会快速推进。
被采用的类器官体系都必须实现标准化。
06
给青年科技工作者寄语
Juliana / 主持人
Juliana:不想扫兴,但节目要收尾了。今天的讨论非常精彩。结束前请 Clevers 教授和林博士给我们一句“总结/寄语”,尤其是给青年科研工作者的建议。
LIN LIN / 林琳
这个问题有点难。我就以“初级PI”的身份给些建议吧。相信听众里有不少新上岗或即将上岗的PI。我做 PI 的第一年,坦白说就像电影《瞬息全宇宙》一样:有大量事情同时向你涌来——建实验室、招人、带学生、写基金、教学、审稿、参加会议出差等等,压力很大。但与此同时,我也觉得持续和别人交流非常重要。比如我很喜欢和 Hans 讨论,虽然他也非常忙,但这种交流会促使我更深入、更有创造性地思考科学,这一点非常重要。这也是一个学习过程:从我自己亲手做实验,转变为同时让很多实验、想法和人一起成长——建设团队、形成科学愿景。我很享受今天的对话,也确实学到了很多,包括从 Hans 那里。最后我想说:去研究类器官吧!
HANS CLEVERS
我经常看到很多博士生和博士后以为当了 PI 之后就是坐在办公室里,别人拿着实验结果进来,你写论文,一切都很轻松。等他们真的当了 PI 之后才发现:当 PI 这件事,比你在一个支持你的 PI 手下做项目要复杂十倍、百倍甚至更多。Lin,你现在应该也体会到了。
如果要给建议,我这些年其实并没有刻意去想“怎么做科学、怎么当 PI”。但回顾我们实验室一路走来的经验,我觉得第一点是:你不可能成为他人的 PI 性格,你只能做你自己。你的个性就是你带到科研、带到 PI 角色里的东西。你可以观察别人,但你必须找到自己的方式。我们的方式是:保持勇气。我们不害怕跳进一个完全陌生、我们几乎一无所知的领域,只要我们能带去一项技术——我们通常就是带着技术去开拓新方向。
我还学到一点:我总会告诉我的人,不要进入那种已经挤满了竞争者、而且大家对“事情应该怎么运作”已经有强烈共识的领域。你需要勇气去走进“黑暗地带”,因为当你在那里面发现新东西时,你会是最早的那批人,你也会有时间去真正搞清楚它是怎么回事。
还有一点很重要:信任。信任你自己,也信任你的同事。不要对坐在你隔壁的博士后藏着掖着你的结果,也不要因为论文没发表就完全不交流,那并不会真正帮助你。这些做法不会让科研变得有趣。我在40年学术科研生涯里,很少很少看到有人会利用你分享的信息来伤害你、占你便宜。相反,分享会不断回报你:你现在帮助了别人,五年后你可能需要对方的帮助,你再联系他/她,别人往往会立刻回馈。所以我觉得:信任、分享、勇气的组合,对我们非常有帮助,也让做科学这件事变得更愉快。