T淋巴细胞作为适应性免疫系统的核心功能细胞,其在抵御病原体感染、清除肿瘤细胞及维持免疫稳态过程中发挥着不可替代的作用。蛋白质合成作为 T 细胞生命活动的基础代谢过程,并非一成不变,而是随着细胞生命周期的推进呈现出精准调控的动态变化特征。
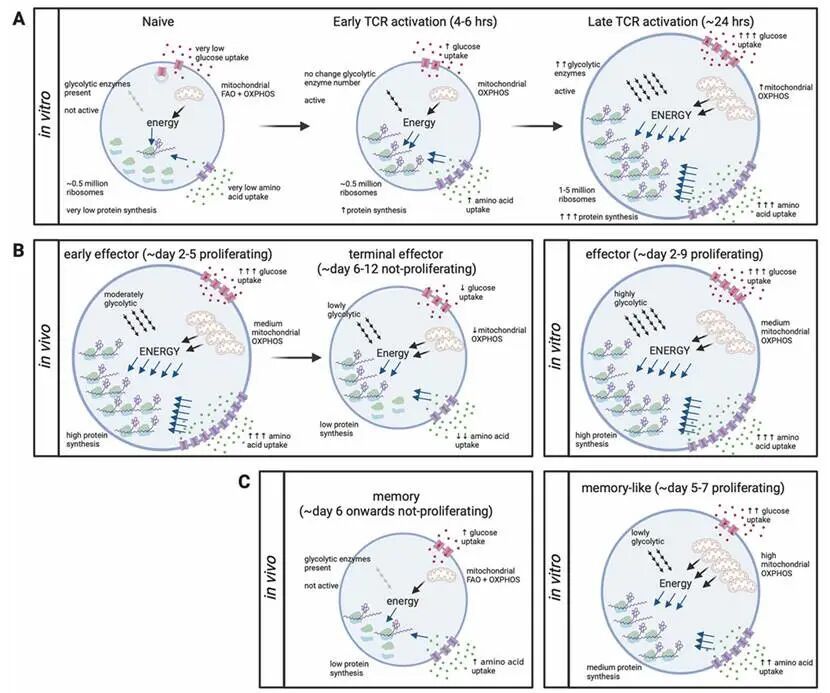
10.1038/s41423-021-00792-8
初始 T细胞:低水平持续合成,维持静息态与应答潜能
初始 T 细胞(Naive T cells)是指尚未接触过特异性抗原的成熟 T 细胞,通常处于细胞周期的 G0/G1 期,被普遍认为是 “静息细胞”。但这一认知并不意味着初始 T 细胞的代谢活动完全停滞,相反,其蛋白质合成以低水平、持续性的模式进行,为细胞的存活、迁移及快速应答潜能提供关键保障。
初始 T 细胞的蛋白质合成速率虽远低于活化 T 细胞,但维持着稳定的合成水平。通过定量高分辨率质谱技术对人 naive CD4 T细胞的蛋白质组进行分析,发现这些细胞中约 7000 种蛋白质中,有 20% 会在 24 小时内完成降解与重新合成的周转过程,据此估算,naive CD4 T 细胞每分钟需合成约 60,000 个蛋白质分子以维持其蛋白质组的稳态。
这种持续的合成活动主要服务于三个核心目的:一是补充维持细胞静息表型的关键转录因子,如KLF2、TCF-1 和 FOXO1 等,这些蛋白质的半衰期较短,需通过持续合成避免其功能缺失;二是维持趋化因子受体和黏附分子的表达,如 CD62L 和 S1P 受体,确保初始T 细胞能够在全身循环中高效迁移至次级淋巴组织,完成抗原识别的 “巡逻” 任务 —— 研究表明,初始 T 细胞 24 小时内可在体内循环多达 4 次,这种高度活跃的迁移能力依赖于相关膜蛋白的稳定表达;三是修复受损的线粒体等细胞器,保障细胞基础代谢的正常运转。
氨基酸作为蛋白质合成的原料,其供应同样受到严格调控。初始 T 细胞主要通过氨基酸转运体从环境中摄取必需氨基酸,如 SLC7A5(负责转运亮氨酸、蛋氨酸等大中性氨基酸)在初始 T 细胞中表达约 10×10³ 拷贝 / 细胞,SLC1A5(谷氨酰胺转运体)的表达量约为 1×10³ 拷贝 / 细胞。此外,自噬过程作为氨基酸供应的补充途径,在初始 T 细胞中也发挥着重要作用,通过降解细胞内衰老或受损的蛋白质,为蛋白质合成提供额外的氨基酸来源,保障合成过程的持续进行。
初始 T 细胞的蛋白质合成调控呈现出“抑制与维持平衡” 的特征。翻译抑制因子 PDCD4 在初始 T 细胞中维持较高水平,约 3×10⁵-5×10⁵拷贝 / 细胞,能够与翻译起始因子 eIF4A1 结合并抑制其活性,从而限制蛋白质合成的整体速率。同时,RNA 结合蛋白如 ZFP36 家族成员和 Roquin1/2 通过调控 mRNA 的稳定性,防止促炎细胞因子等蛋白的异常表达,维持初始 T 细胞的静息表型。这种精细的调控网络确保初始 T 细胞在未受抗原刺激时,既不浪费能量进行大量蛋白质合成,又能保持足够的合成活性以应对潜在的免疫挑战。
活化 T细胞:合成水平激增,支撑增殖与效应功能
当初始 T 细胞通过 T 细胞受体(TCR)识别抗原 - MHC 复合物,并获得 CD28 等共刺激信号后,会迅速启动免疫活化程序,蛋白质合成也随之进入 “爆发式” 增长阶段。这一阶段的蛋白质合成不仅速率大幅提升,还伴随着蛋白质组的全面重塑,为 T 细胞的快速克隆扩增、效应分子产生及功能分化提供核心支撑。
活化 T 细胞的蛋白质合成水平呈现显著的量级提升。研究显示,小鼠 CD8 T 细胞在抗原激活 24 小时内,细胞质量可增至初始状态的 3 倍;而体外培养的 CD8 效应细胞毒性 T 细胞,其总蛋白质量是初始淋巴细胞的 4 倍。CD4 T 细胞的蛋白质合成同样显著上调,尽管其蛋白质量比同期激活的 CD8 T 细胞低 20%-30%,但仍较初始状态大幅增加。从蛋白质丰度变化来看,激活 24 小时内,CD4 和 CD8 T 细胞中分别有5400-6300 种蛋白质的丰度显著上升,而效应 CD8 细胞毒性 T 细胞和 CD4 Th1 细胞较初始T 细胞上调的蛋白质种类更是超过 7000 种,涵盖了驱动效应分化的转录因子、颗粒酶和穿孔素等免疫效应分子、细胞因子受体、细胞周期核心蛋白及代谢酶类等多个功能类别。
蛋白质合成的激增为 T 细胞的两大核心功能提供保障:一是快速克隆扩增。在 optimal 免疫刺激下,T 细胞需约 18 小时从 G0 期退出并进入 G1期启动 DNA 复制,随后进入快速分裂阶段,48 小时内可完成 4-6 次细胞分裂。细胞分裂过程中,子代细胞需继承与母细胞相当的细胞质量,这就要求活化T 细胞通过高效的蛋白质合成,在每次分裂前将细胞质量翻倍,为子代细胞的形成提供物质基础。二是效应功能的实现。效应 CD8 T 细胞作为 “serial killer 细胞”,需持续合成细胞毒性颗粒相关的颗粒酶 B、穿孔素等,其中颗粒酶 B 在效应 CD8 T 细胞中的表达量可高达 2000 万拷贝 / 细胞,这种高效合成确保了 T 细胞能够快速清除被病原体感染的细胞或肿瘤细胞。效应 CD4 T 细胞则需合成大量细胞因子和趋化因子,如 IL-2、TNF-α 等,这些分子在激活后 2-3 小时即可被检测到,通过调控免疫微环境协调整体适应性免疫应答。
活化 T 细胞蛋白质合成的上调依赖于翻译机器的全面重塑。核糖体作为蛋白质合成的核心场所,其数量在 T 细胞活化后可增至初始状态的 10 倍,同时形成多核糖体结构,显著提升 mRNA 的翻译效率。翻译起始复合体的表达也发生显著变化:eIF4F 复合体(由 eIF4A、eIF4E 和 eIF4G组成)的各组分表达上调,其中 eIF4A1 的拷贝数增加 10倍;而翻译抑制因子 PDCD4 的表达则下降 5-10 倍,导致 PDCD4 与 eIF4A1 的比例大幅降低,解除了对 cap 依赖翻译的抑制。此外,活化 T 细胞还会增强核糖体 RNA 的合成,上调氨酰 - tRNA 合成酶的表达,并积累具有功能活性的 eIF5A(通过 hypusination 修饰实现),从多个层面提升翻译机器的工作效率。
RNA 修饰在活化 T 细胞的蛋白质合成调控中也发挥着关键作用。mRNA 的 5' 端 m⁷G 帽甲基化由 RNA 帽甲基转移酶RNMT 及其辅因子 RAM 介导,活化 T 细胞中这两种蛋白的表达显著上调,确保 mRNA 的稳定性和核糖体招募效率;而 N⁶- 甲基腺苷(m⁶A)修饰作为另一种重要的 RNA 修饰方式,由 METTL3 催化,参与调控 mRNA 的翻译、剪接和稳定性,METTL3 缺陷的 T 细胞无法正常分化为效应细胞,凸显了 RNA 修饰对蛋白质合成的重要调控作用。
记忆 T细胞:合成水平回落,保留快速响应潜能
当病原体被清除、抗原刺激消失后,大部分效应 T 细胞会发生凋亡,仅有少数细胞存活并分化为记忆 T 细胞(Memory T cells)。与效应 T 细胞的高合成状态不同,记忆 T 细胞的蛋白质合成水平回落至接近初始 T 细胞的水平,但仍保持独特的动态特征,使其能够在二次感染时快速启动回忆应答。
记忆 T 细胞的蛋白质合成呈现“低水平、高灵活性” 的特征。研究发现,外周血记忆 T细胞的蛋白质周转效率比初始 T 细胞高 80%,尽管其整体合成速率仍远低于效应 T 细胞,但这种高效的周转能力确保了细胞能够快速更新关键蛋白,维持长期存活和应答潜能。与初始 T 细胞类似,记忆 T 细胞的蛋白质合成主要用于维持细胞稳态、修复细胞器及表达趋化因子受体和黏附分子,但其合成调控更具 “可塑性”—— 当再次遭遇相同抗原刺激时,记忆 T 细胞可在短时间内启动蛋白质合成的快速上调,其核糖体生物发生和翻译机器激活的速度显著快于初始 T 细胞,从而能够更快地增殖分化为效应细胞,产生更强的免疫应答。
记忆 T 细胞的蛋白质合成依赖于特定的细胞因子信号和代谢适应。IL-7 和 IL-15 是维持记忆 T细胞存活和合成稳态的关键细胞因子:IL-7 通过调控抗凋亡蛋白的表达和代谢酶活性,为蛋白质合成提供能量和原料支持;IL-15 则参与调控核糖体相关基因的表达,维持记忆 T 细胞的翻译潜能。在代谢模式上,记忆 T 细胞采用氧化磷酸化与糖酵解并存的 “代谢柔性” 策略,线粒体功能得到优化,能够高效利用葡萄糖、脂肪酸等多种营养物质,为低水平但持续的蛋白质合成提供能量保障。此外,自噬过程在记忆 T 细胞中持续激活,通过降解细胞内蛋白质产生氨基酸,补充外源性氨基酸摄取的不足,确保蛋白质合成的稳定进行。
记忆 T 细胞的蛋白质合成调控还涉及翻译机器的 “预储备”。研究表明,记忆 T 细胞中保留了一定水平的核糖体和翻译起始因子,如 eIF4F 复合体的关键组分,同时翻译抑制因子的表达维持在适度水平,既避免了不必要的能量消耗,又能在二次激活时快速解除抑制。此外,记忆 T 细胞中 RNA 帽甲基化相关蛋白和氨基酸转运体的表达也维持在基础水平,如 SLC7A5、SLC2A1 等转运体的表达量虽低于效应 T 细胞,但高于初始 T 细胞,为快速上调的合成需求做好物质准备。
耗竭 T 细胞
耗竭 T 细胞是在慢性感染或肿瘤微环境中形成的功能缺陷性 T 细胞,其特征是细胞因子产生能力下降、效应功能减弱,且高表达 PD-1、Tim-3 等共抑制受体。尽管耗竭 T 细胞的蛋白质合成特征尚未被系统解析,但现有研究提示,合成功能缺陷可能是其功能耗竭的重要原因之一。在肿瘤微环境中,T 细胞需与肿瘤细胞、肿瘤浸润髓系细胞竞争葡萄糖、氨基酸等营养物质,导致营养供应不足,进而限制蛋白质合成所需的原料和能量;同时,共抑制受体信号可能阻断抗原受体和细胞因子介导的合成激活通路,导致核糖体生物发生受阻、氨基酸转运体表达下调,最终影响效应分子的合成。此外,耗竭 T 细胞的转录组重编程可能直接影响 Myc 等核心调控因子的表达,进一步削弱蛋白质合成能力。验证蛋白质合成缺陷是否为 T 细胞耗竭的核心机制,以及如何通过调控合成过程逆转耗竭状态,将为肿瘤免疫治疗提供新的思路。
参考资料
Linda V Sinclair, Doreen A Cantrell,Protein Synthesis and Metabolism in T Cells,Annu Rev Immunol. 2025 Apr;43(1):343-366. doi: 10.1146/annurev-immunol-082323-035253.
Julia M Marchingo , Doreen A Cantrell ,Protein synthesis, degradation, and energy metabolism in T cell immunity,Cell Mol Immunol. 2022 Mar;19(3):303-315. doi: 10.1038/s41423-021-00792-8
Solt LA (2022) Emerging insights and challenges for understanding T cell function through the proteome.Front. Immunol. 13:1028366.doi: 10.3389/fimmu.2022.1028366

