疫苗在控制传染病方面发挥了巨大作用,近几年更是帮助遏制了COVID-19 新冠大流行。
预防性癌症疫苗通过抵御致癌病原体,已阻止了多种恶性肿瘤的发生。与之相对,治疗性疫苗训练免疫系统清除已形成的肿瘤,已经在临床中展现出良好前景。
在辅助阶段,抗黑色素瘤和胰腺癌的疫苗似乎正在减少微小残留病灶并降低复发率;在大转移阶段,原位疫苗已使晚期肺癌、乳腺癌及淋巴瘤出现系统性消退。
凭借对肿瘤免疫学关键细胞因子的深入理解、新型疫苗组分的高效动员与激活能力、组学与人工智能在疫苗设计中的应用,以及免疫检查点抑制剂的联合使用,更有效的新一代癌症疫苗正在诞生。
今天一起看看癌症疫苗临床试验、不同疫苗策略的优势与局限,下一代癌症疫苗如何帮助改善患者的疗效与生活质量。
主要内容
1、治疗性肿瘤疫苗的类型
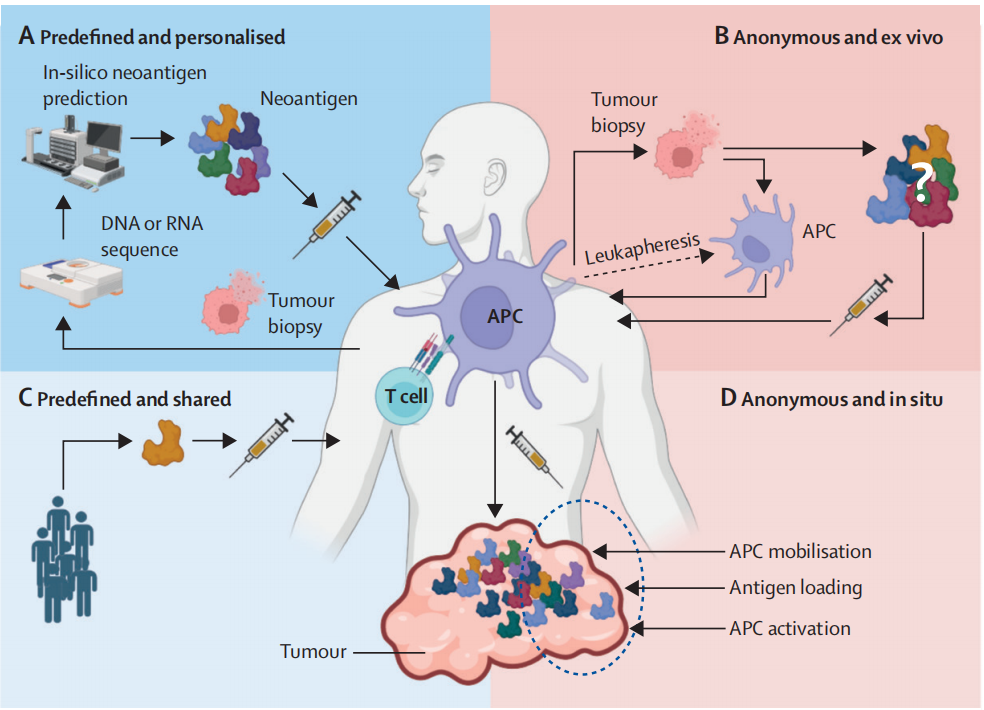
治疗性肿瘤疫苗的类型
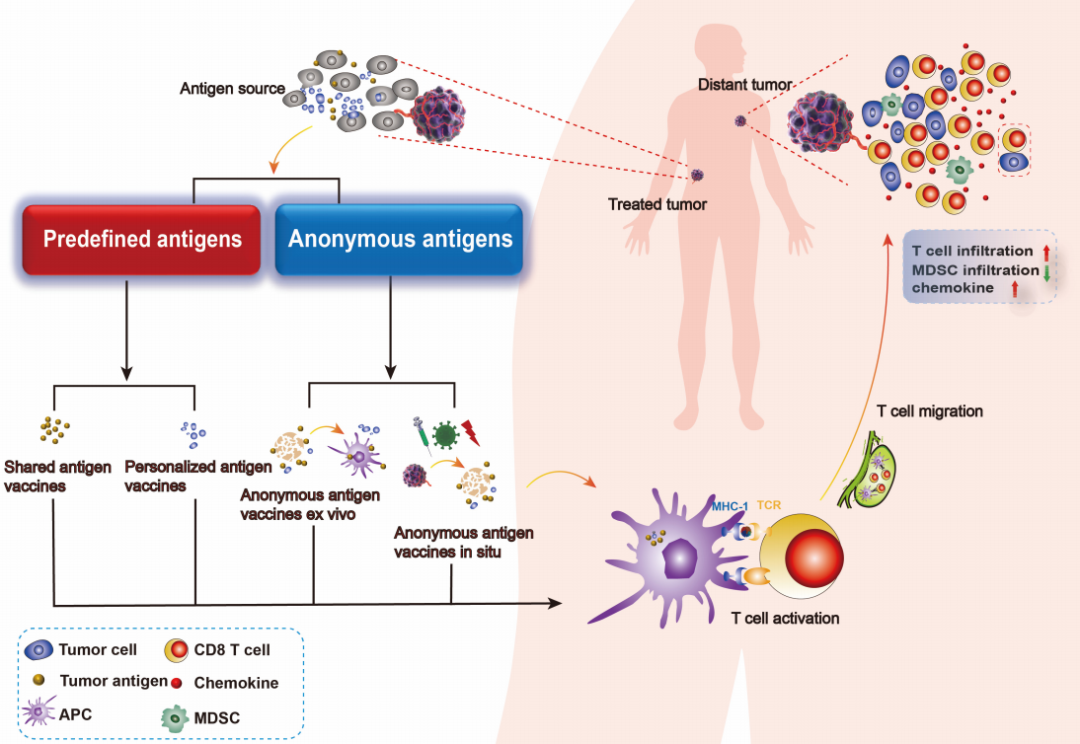
疫苗可根据“抗原如何被选取”以及“抗原在哪里与抗原提呈细胞(APCs)共定位”进行分类。
(A) Predefined-个体化:获取患者自身肿瘤并加工成新抗原,用以制备个体化疫苗。
(B) 广谱-体外:采集患者肿瘤制成裂解物,再将裂解物负载于自体APCs后回输,或经免疫原性增强处理后重新包装并全身回输。
(C) Predefined-共享:利用在多个患者同种肿瘤中高表达的共有抗原开发疫苗。
(D) 广谱-原位:不切除肿瘤,而是在体内通过联合疗法直接作用于肿瘤,实现原位疫苗效应。
肿瘤疫苗由肿瘤抗原制备而成,因此可激活特异性抗肿瘤免疫应答,包括提高肿瘤内趋化因子的表达、增加T细胞浸润并减少髓源性抑制细胞(MDSC)的浸润。根据肿瘤抗原来源的不同,疫苗可分为“特异性抗原疫苗-Defined-antigen vaccines”和“广谱抗原疫苗-Anonymous-antigen vaccines”。
特异性抗原疫苗包括共享抗原疫苗和个体化抗原疫苗,二者均需事先制备特定的肿瘤抗原。
广谱抗原疫苗包括体外匿名抗原疫苗和体内匿名抗原疫苗,它们利用患者体内的全部肿瘤抗原谱作为疫苗来源。
2、目前获批上市的肿瘤疫苗
FDA批准的治疗性肿瘤疫苗共有4个
卡介苗(BCG):减毒的牛型结核分枝杆菌活疫苗,最早1990年获批用于非肌层浸润性膀胱癌(NMIBC)的膀胱灌注治疗,通过将减毒结核菌直接灌注膀胱,被免疫细胞识别后引发"炎症风暴",大量激活T细胞、巨噬细胞等吞噬癌细胞,类似"以毒攻毒"的局部免疫刺激。至今,卡介苗仍是治疗非肌层浸润性膀胱癌的标准方案,临床应用非常成熟。也是预防结核病的预防性细菌疫苗。
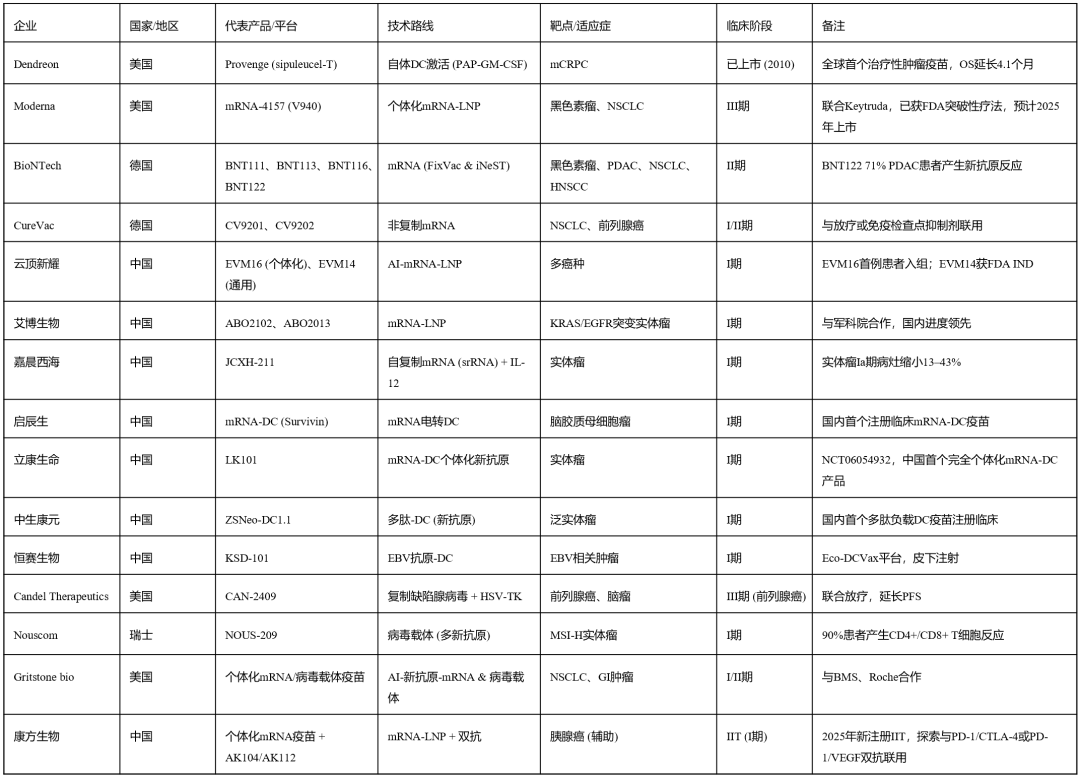
Sipuleucel-T(Provenge): 自体树突状细胞疫苗,2010年4月获批治疗无症状或症状较轻的转移性去势抵抗性前列腺癌(mCRPC),抽取患者血液分离树突状细胞(抗原递呈细胞),在体外用前列腺肿瘤抗原"训练"后回输体内,教会免疫系统识别并攻击表达该抗原的癌细胞。
Talimogene laherparepvec(T-VEC,Imlygic):溶瘤病毒疫苗,2015年10月获批用于手术无法切除且术后复发的黑色素瘤患者的皮肤、皮下及淋巴结病灶的局部治疗,将基因改造的疱疹病毒直接注射到皮肤肿瘤内,只在癌细胞内复制并杀死它们(溶瘤),同时释放GM-CSF因子招募免疫细胞,形成"就地疫苗"效应触发全身抗肿瘤反应。
Nadofaragene firadenovec(Adstiladrin):腺病毒疫苗,2022年12月获批用于治疗患有原位癌(伴或不伴乳头状肿瘤)的高风险、对卡介苗(BCG)治疗无反应的非肌层浸润性膀胱癌(NMIBC)成年患者,利用腺病毒作为"快递盒",将干扰素基因送入膀胱细胞,使其持续分泌IFN-α蛋白激活免疫警钟,专门用于BCG治疗失败后的患者,重新唤醒抗肿瘤免疫力。是第一个获得FDA批准的腺病毒载体基因疗法。
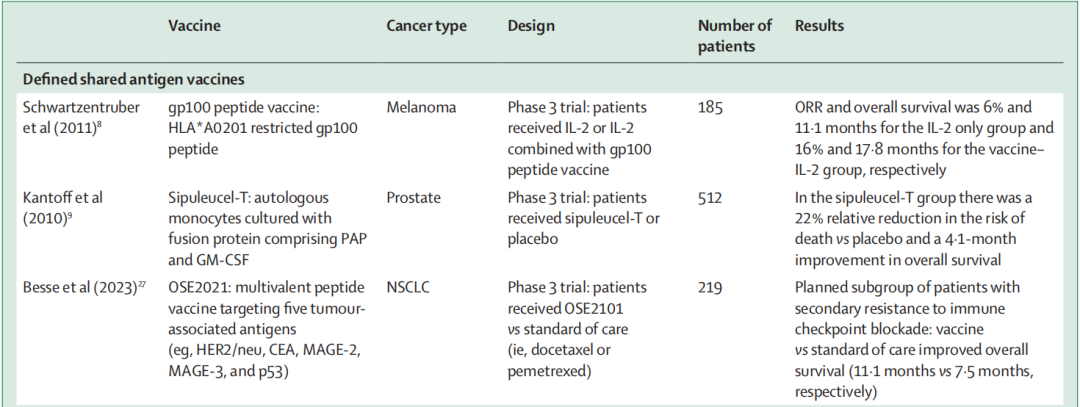
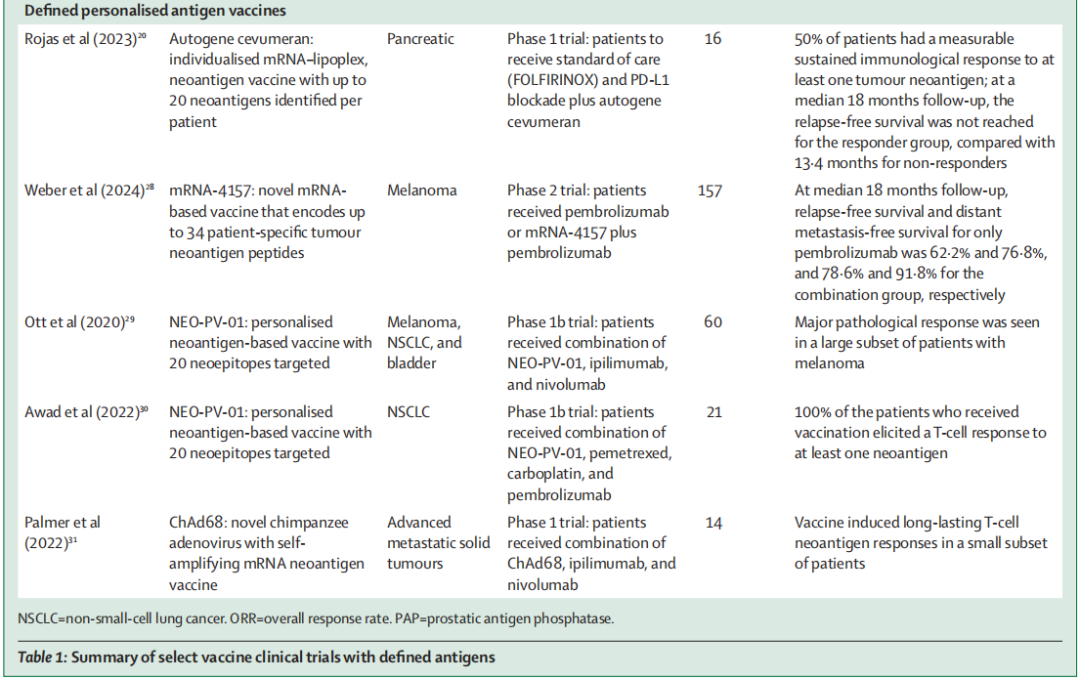
部分特定Defined抗原的疫苗临床试验小结
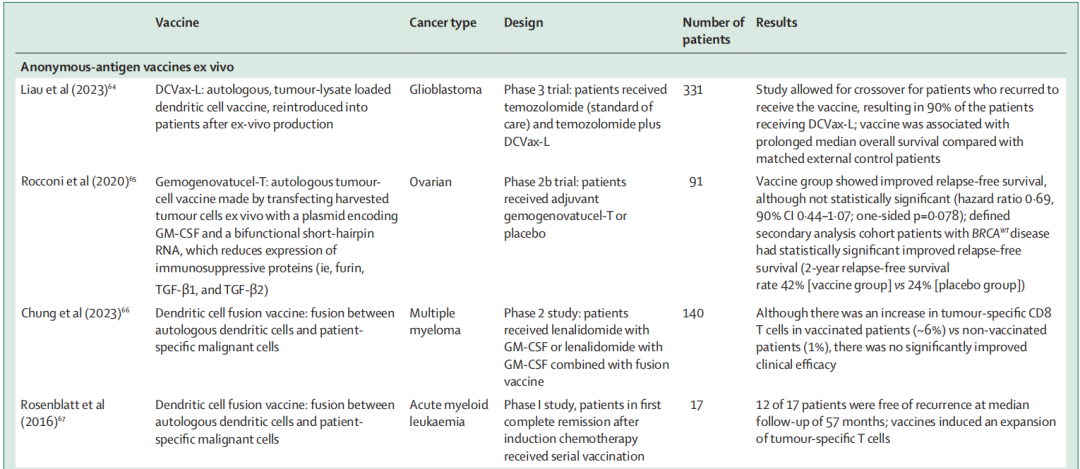
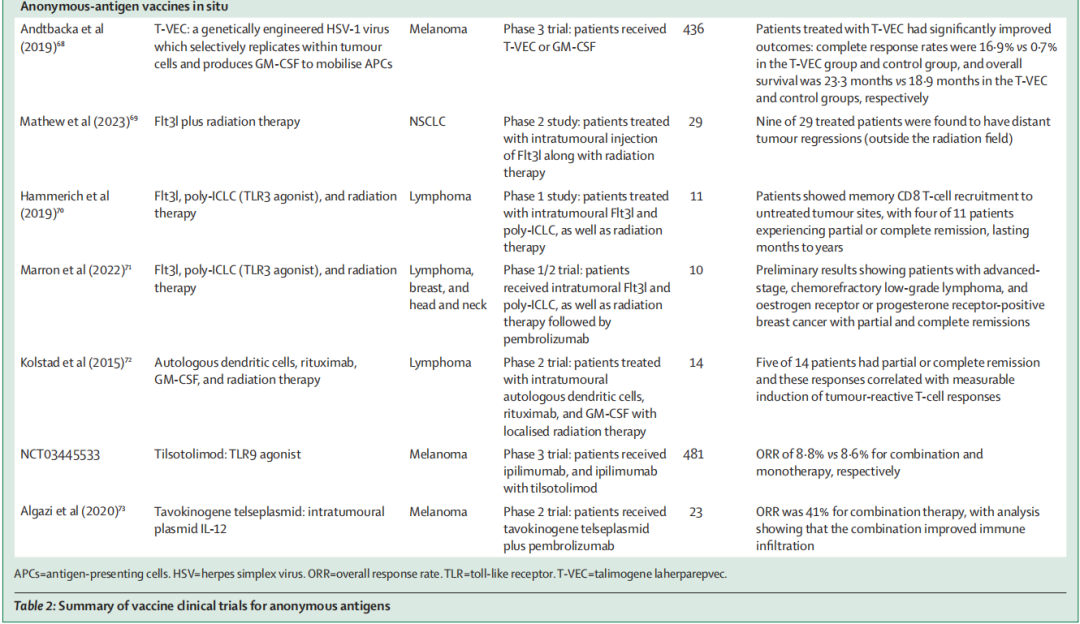
3、针对广谱Anonymous抗原的疫苗临床试验总结
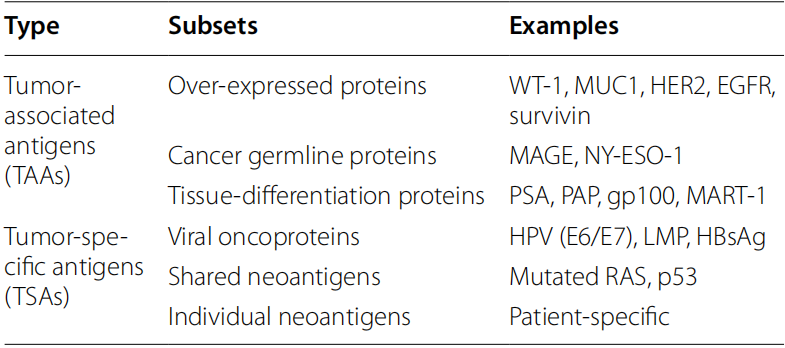
4、抗原分类
5、新抗原识别流程与来源
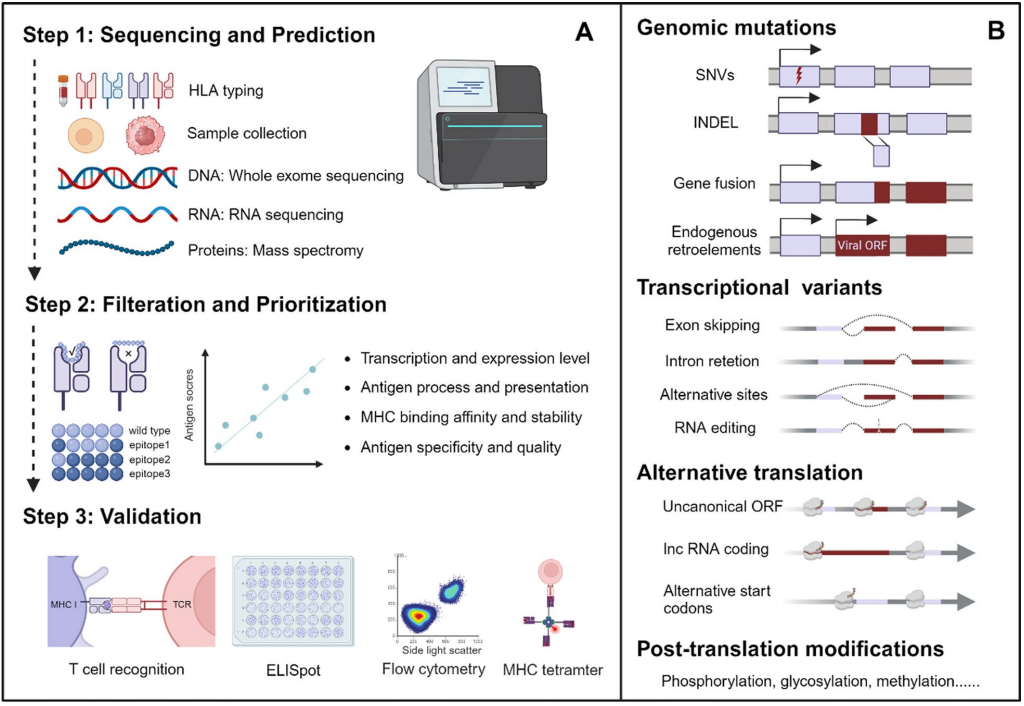
A新抗原的预测过程遵循一个系统的三步流程:预测阶段通过肿瘤 DNA、RNA 和蛋白质测序,利用计算工具根据患者的HLA分型来识别肿瘤特异性突变;筛选阶段根据诸如表达水平、被处理和呈递在主要组织相容性复合体(MHC)上的可能性、MHC 结合亲和力以及抗原特异性等特征对预测的新抗原进行排序;验证阶段通过实验方法来确认新抗原引发特异性 T 细胞反应的能力。
B新抗原来源于多种机制,包括基因组改变(如点突变、基因融合和缺失)、异常转录事件、选择性剪接或翻译以及后翻译修饰。这些机制产生了在正常组织中不存在的肿瘤特异性抗原,使其成为个性化癌症免疫疗法的理想靶点,这些疗法旨在诱导精确的免疫反应。
6、癌症疫苗诱导的免疫反应
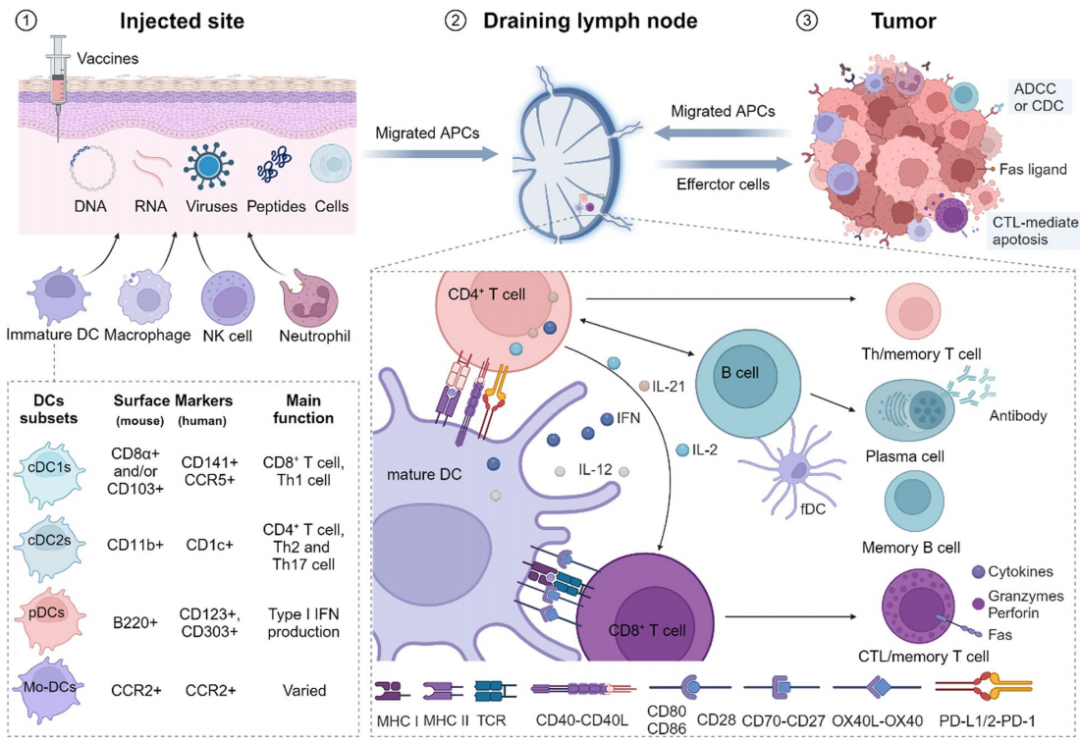
(1)接种疫苗后,抗原呈递细胞(APC),尤其是树突状细胞(DC),会捕获、处理并将其表面的抗原呈递给其他细胞。不同的树突状细胞亚群具有不同的激活特定T细胞亚群的能力。随着树突状细胞的成熟,它们会迁移到诸如引流淋巴结之类的次级淋巴器官中。
(2)要实现有效的T细胞激活,需要三个关键信号。信号 1 是抗原-MHC 复合物在 APC 和 T 细胞受体之间的结合。信号 2 包括共刺激分子,它们会放大激活信号。信号 3 由免疫调节细胞因子和趋化因子组成,这些因子会影响 T 细胞的分化和功能。一旦激活,T 细胞会分化为效应细胞,包括 CD4 辅助性 T(Th)细胞、细胞毒性 CD8T细胞(CTL)和记忆 T 细胞。CD4+T细胞与滤泡树突状细胞(fDCs)一起协助 B 细胞的成熟,从而分化为产生抗体的浆细胞和记忆 B 细胞。
(3)被激活的免疫细胞会侵入肿瘤并发挥抗肿瘤作用。CTLs(细胞毒性T淋巴细胞)通过穿孔素、颗粒酶和Fas配体的结合来诱导肿瘤细胞凋亡,而B细胞则利用抗体依赖性细胞毒性(ADCC)和补体依赖性细胞毒性(CDC)来发挥作用。肿瘤浸润的抗原呈递细胞还能将抗原呈递给机体,从而增强针对肿瘤的细胞免疫反应。
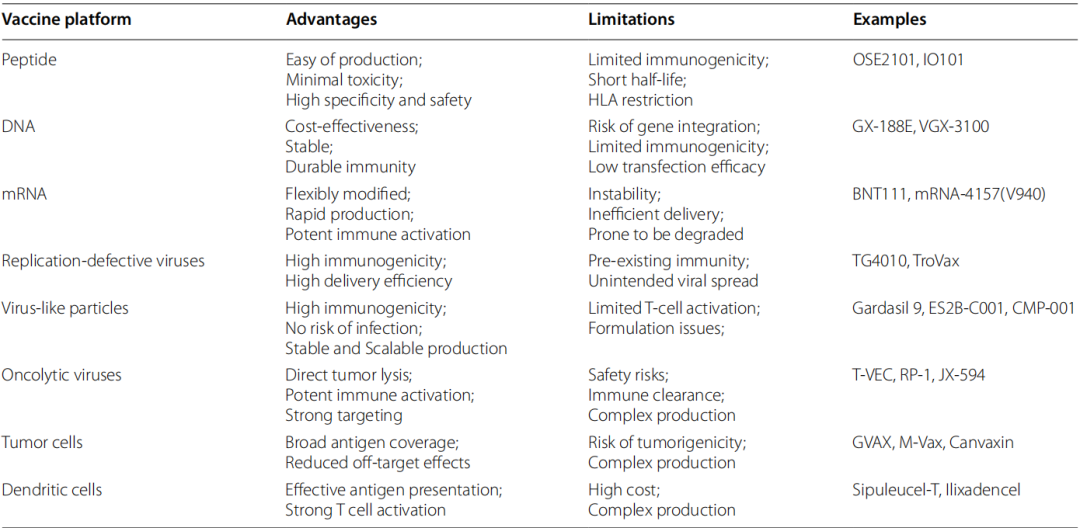
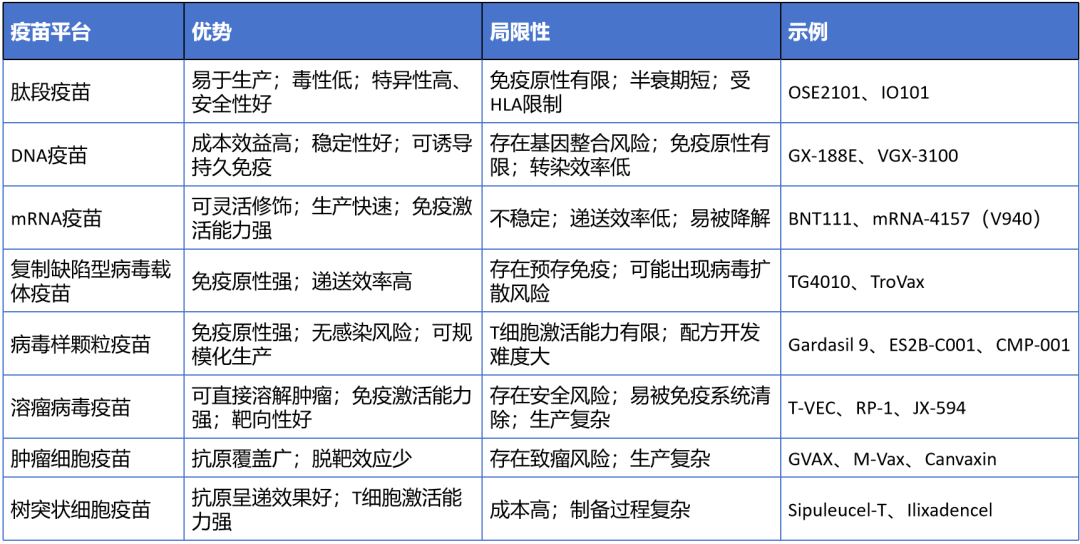
7、不同肿瘤疫苗平台特征
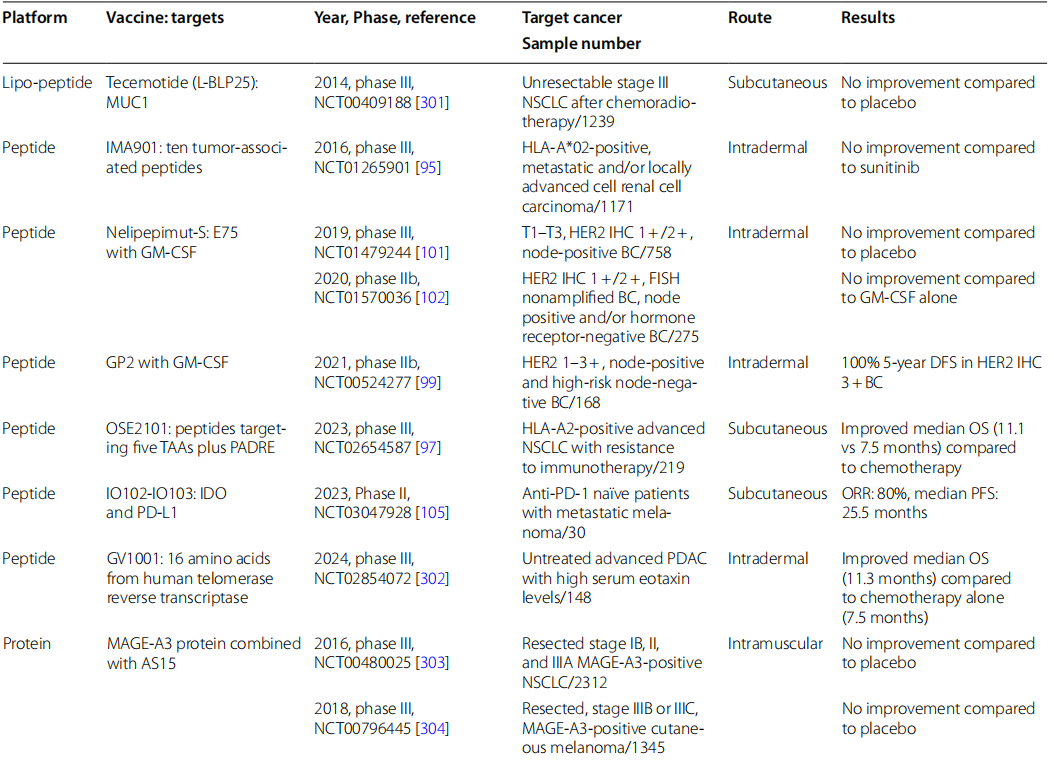
8、基于肽/蛋白质的癌症疫苗的 II 期至 III 期临床试验
多数疫苗可诱导免疫反应,但临床疗效不一;
OSE2101在NSCLC中延长OS(11.1 vs 7.5个月);
E75、GP2等乳腺癌疫苗部分有效,III期结果不佳;
IO102-IO103(IDO/PD-L1)联合PD-1治疗黑色素瘤ORR达80%。
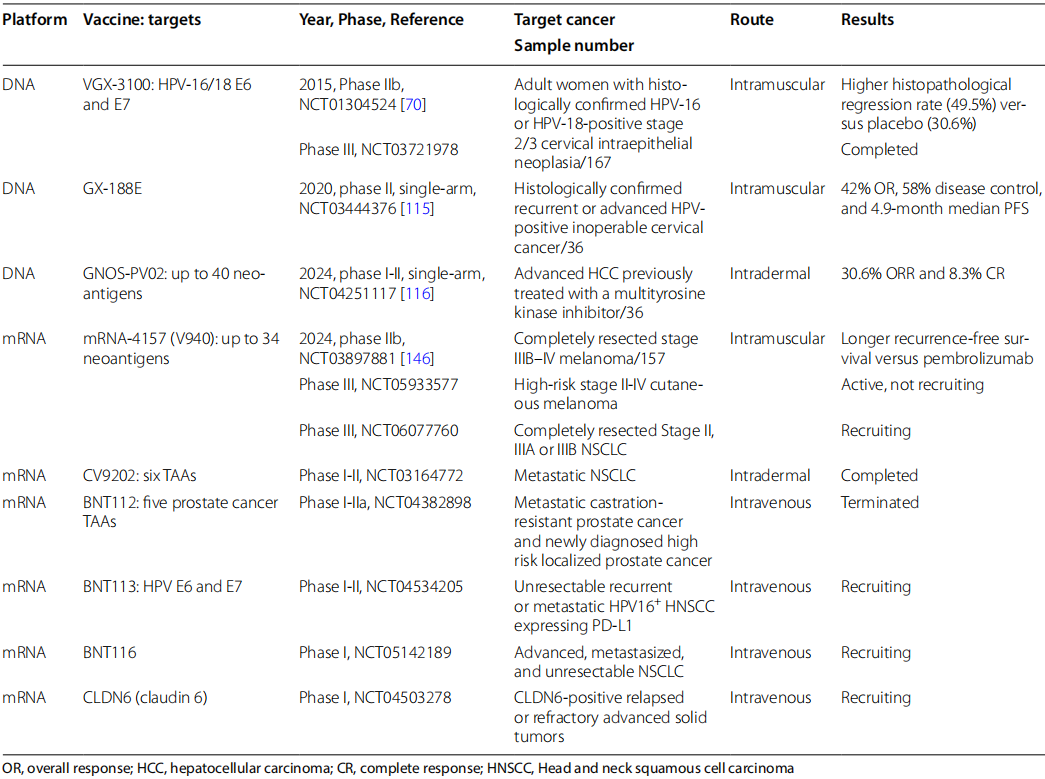
9、核酸疫苗(DNA/mRNA)临床试验结果
VGX-3100(DNA)治疗宫颈病变有效,III期成功;
mRNA-4157联合PD-1显著降低黑色素瘤复发率;
BNT111、BNT122等mRNA疫苗在PD-1耐药患者中显示疗效;
个别试验(如mRNA-5691)因疗效不佳终止。
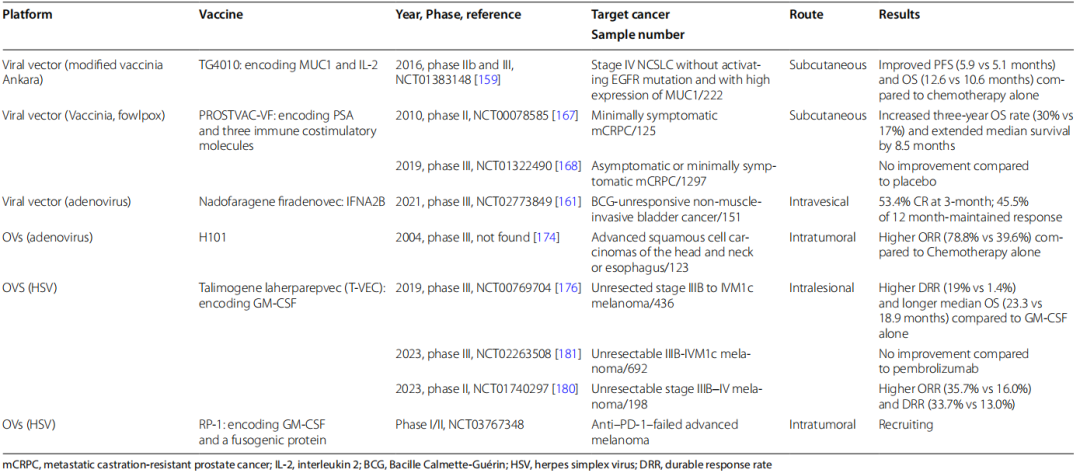
10、基于病毒的癌症疫苗的II 期至 III 期临床试验
TG4010(MVA载体)联合化疗改善NSCLC患者OS;
T-VEC(溶瘤HSV)联合PD-1未能改善黑色素瘤疗效;
RP-1联合nivolumab在PD-1耐药黑色素瘤中ORR约33%,中位缓解期21.6个月;
nadofaragenefiradenovec(Ad载体)已获批用于膀胱癌。
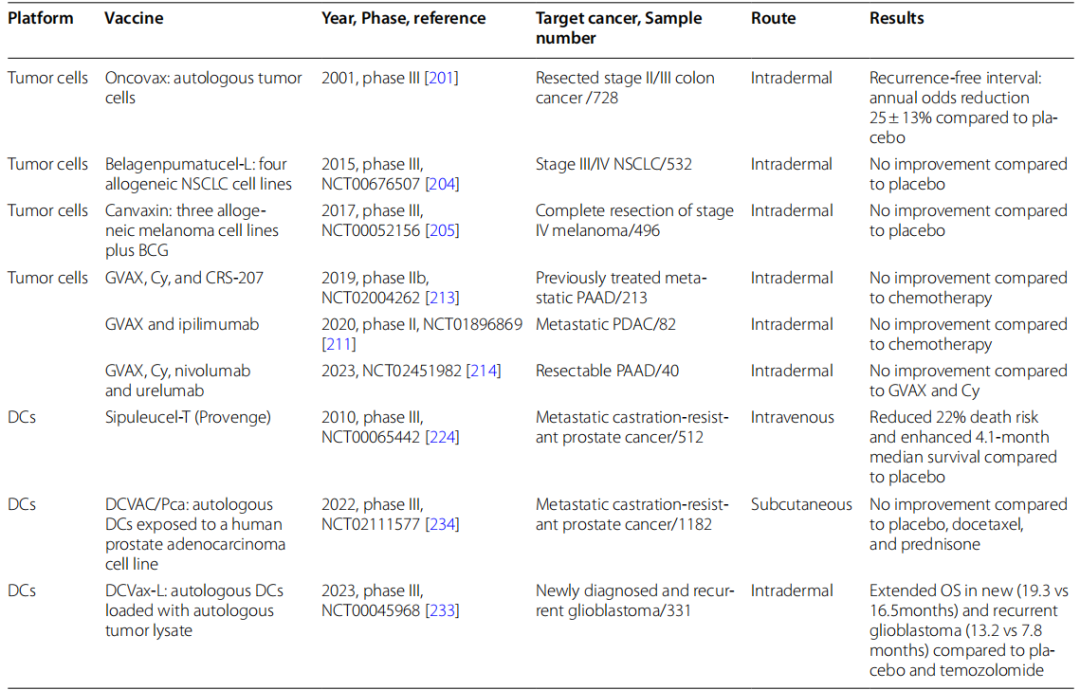
11、基于细胞的癌症疫苗的 II 期至 III 期临床试验
细胞疫苗(肿瘤细胞/DC)临床试验结果
普列威(Provenge,通用名Sipuleucel-T)是全球首个获批(2010年)的前列腺癌治疗性疫苗,属于自体细胞免疫疗法;
DCVax-L(DC加载肿瘤裂解物)显著延长胶质母细胞瘤生存期;
GVAX系列疫苗免疫原性好,但多数III期试验未达主要终点;
Ilixadencel(异体DC)联合sunitinib提高肾癌ORR(42.2% vs 24.0%)。
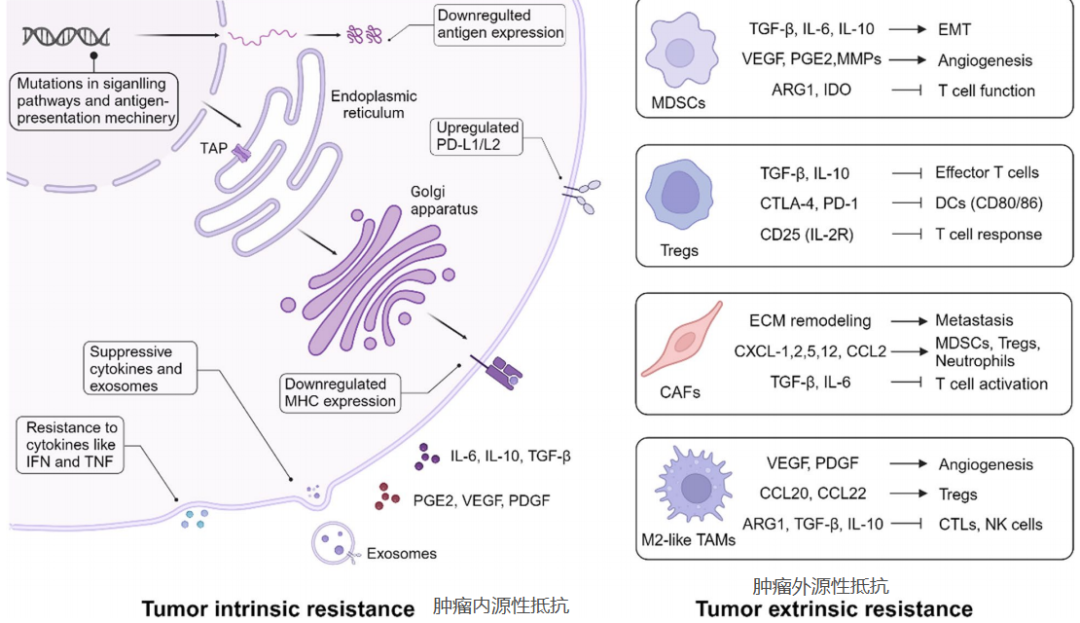
12、肿瘤对疫苗治疗的抗性机制
肿瘤对疫苗治疗的耐药机制
内在:抗原丢失、MHC突变、信号通路异常(如IFN通路缺失);
外在:免疫抑制微环境(Treg、MDSC、CAF、M2-TAM等)、免疫检查点上调、抑制性细胞因子(如TGF-β、IL-10)等。
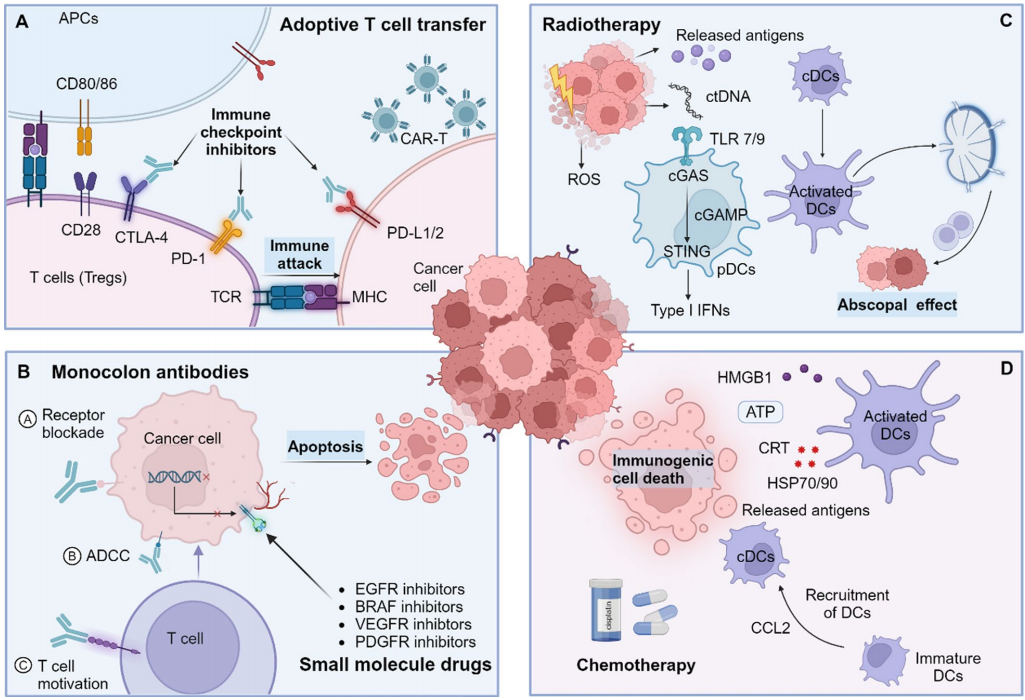
13、联合治疗增强疫苗疗效的机制
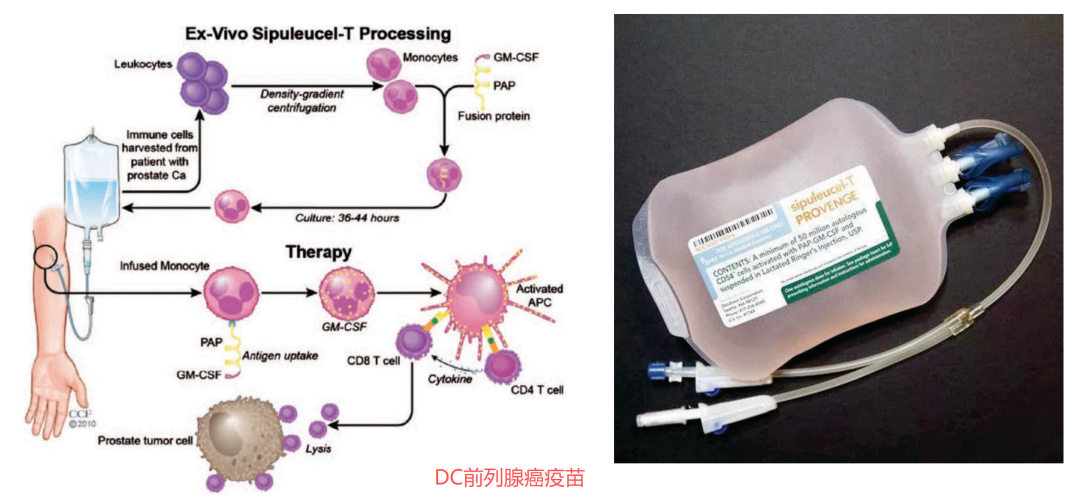
免疫检查点抑制剂:解除T细胞抑制;
化疗/放疗:诱导免疫原性细胞死亡,释放DAMPs,激活DC;
靶向药物:增强抗原呈递或抑制免疫抑制因子;
细胞治疗(如CAR-T):疫苗可增强其活性与持久性。
14布局肿瘤疫苗的部分企业
附3个疫苗作用机制
Sipuleucel-T,自体树突状细胞疫苗
15OSE2101(Tedopi):新抗原癌症疫苗,作用机制
Tedopi靶向针对肺癌细胞中高表达的5种肿瘤相关抗原(CEA、p53、HER-2、MAGE-A2和MAGE-A3),再从这5种与肿瘤相关的抗原中选择和优化的10种新表位的专有组合,可以更好的刺激T淋巴细胞识别和攻击癌细胞。
2008年一项 II 期临床研究结果显示,Tedopi治疗晚期NSCLC 患者的中位 OS 达到 17.3个月。
2023年2月15日,OSE Immunotherapeutics(简称OSE)宣布癌症疫苗Tedopi获FDA和EMA同意开展验证性III期临床,用于二线治疗HLA-A2阳性晚期非小细胞肺癌(NSCLC)。该研究完成后,其结果将作为Tedopi新药申请材料的一部分。
2025年3月11日,OSE Immunotherapeutics和GERCOR共同宣布治疗性治疗疫苗OSE-2101(Tedopi)在晚期胰腺癌(PDAC,胰腺导管腺癌)II期临床TEDOPaM(GERCOR D17-01 PRODIGE 63)中获得积极顶线结果。
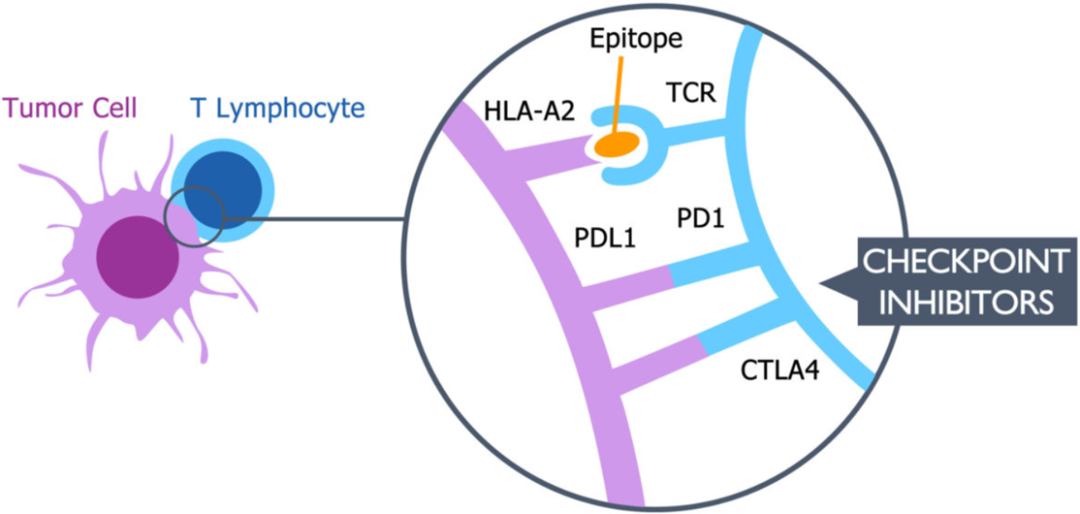
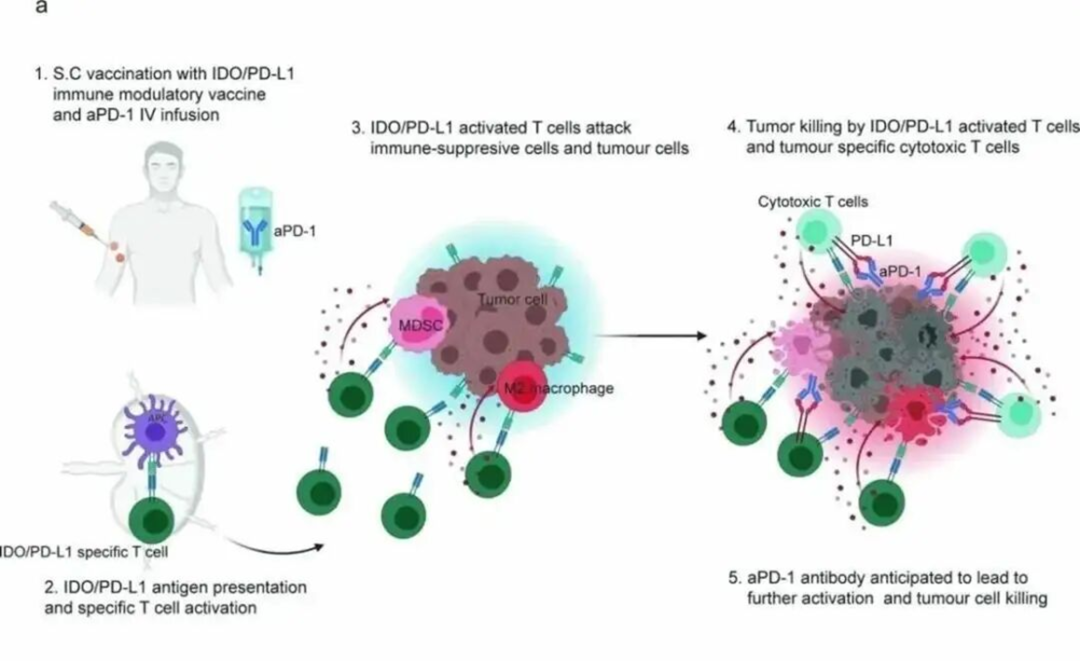
IO101是IO102/IO103(现名Cylembio)疫苗的早期编号,作用机制
Cylembio(疫苗包含两种合成肽表位imsapepimut和etimupepimut),又称IO102-IO103,imsapepimut靶向IDO1和etimupepimut靶向PD-L1,,通过佐剂皮下注射后,被抗原呈递细胞(APC)摄取并呈递。
2025年8月10日,IO Biotech宣布PD-L1/IDO1癌症疫苗Cylembio(IO102-IO103)的III期IOB-013(KEYNOTE-D18)研究未达到主要终点。