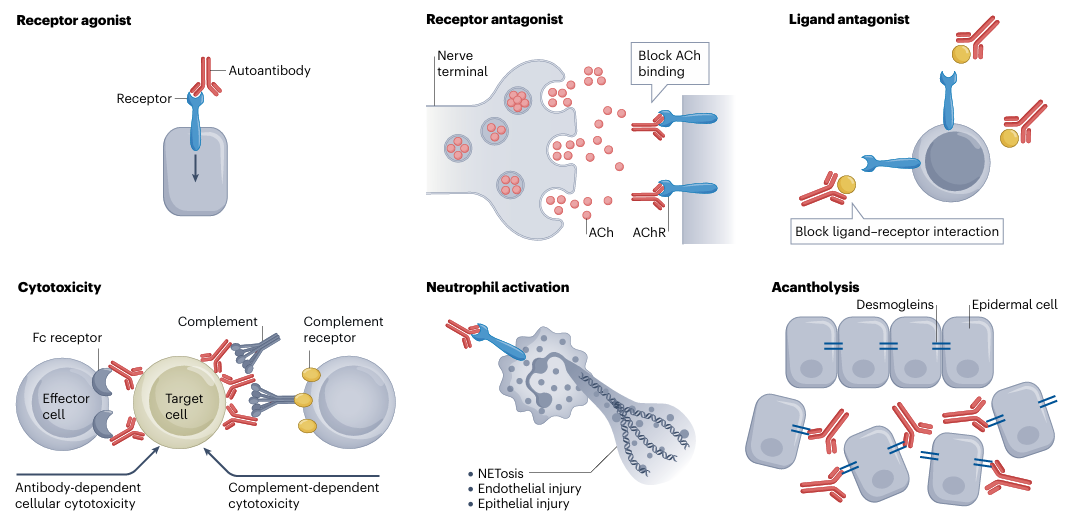
自身抗体是机体免疫系统对自身组织成分产生的特异性免疫球蛋白,其产生与自身免疫耐受破坏密切相关,不仅是自身免疫病的重要标志物,更在疾病发生发展中发挥关键作用。
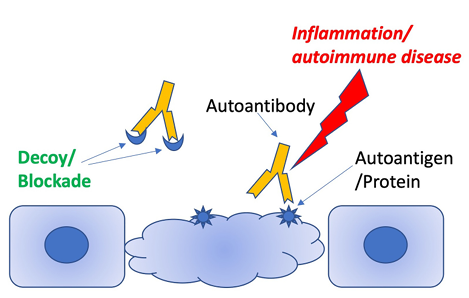
10.3389/fimmu.2022.812649
抗核抗体谱(15 种):系统性自身免疫病的核心标志物
抗核抗体谱(ANAs)是针对细胞核内核酸、核蛋白及核结构成分的一类抗体总称,主要关联系统性红斑狼疮(SLE)、干燥综合征(SS)、系统性硬化症(SSc)等系统性自身免疫病,是临床筛查与确诊的核心指标。
1. 抗核抗体(ANA)
靶抗原
细胞核内所有核酸和核蛋白(如 DNA、组蛋白、核小体等)的总称,无特异性靶抗原,仅反映核成分的免疫反应。
临床关联
自身免疫病的 “筛查指标”,阳性率在 SLE 中达 95%~100%、干燥综合征中达 80%~90%、类风湿关节炎(RA)中达 30%~50%,但健康人群(尤其老年女性)也可能出现低滴度阳性(<1:80),需结合其他指标判断。
检测意义
阴性可基本排除多数系统性自身免疫病(敏感性 95% 以上),阳性需进一步检测特异性抗体(如抗 dsDNA、抗 Sm)明确诊断。
2. 抗双链 DNA 抗体(抗 dsDNA)
靶抗原
细胞核内双链 DNA(天然 DNA),仅识别双链结构,不与单链 DNA 反应。
临床关联
SLE 的 “特异性标志物”,阳性率约 60%~90%,且抗体滴度与 SLE 疾病活动度直接相关 —— 滴度升高常提示肾脏受累(狼疮肾炎)、皮疹加重,滴度下降多为病情缓解标志。
检测意义
特异性达 95% 以上,是 SLE 诊断(2019 年 EULAR/ACR 分类标准)的关键指标,也是监测狼疮肾炎治疗效果的核心依据。
3. 抗单链 DNA 抗体(抗 ssDNA)
靶抗原
细胞核内单链 DNA(变性 DNA),可与 RNA 交叉反应。
临床关联
多见于 SLE(阳性率 50%~70%),也可见于干燥综合征、类风湿关节炎,特异性较低(约 60%),无法单独作为 SLE 确诊依据。
检测意义
常与抗 dsDNA 同时阳性,可辅助判断 SLE 病情活动,但单独阳性临床价值有限。
4. 抗核小体抗体(抗 nucleosome)
靶抗原
细胞核内核小体(由组蛋白与双链 DNA 组成的核心颗粒),是 DNA 损伤后释放的关键自身抗原。
临床关联
SLE 的早期诊断标志物,阳性率约 50%~80%,尤其在抗 dsDNA 阴性的 SLE 患者中阳性率较高(约 40%),也与狼疮肾炎的发生密切相关。
检测意义
弥补抗 dsDNA 的漏诊风险,对早期 SLE 或不典型 SLE 的诊断有重要补充价值。
5. 抗组蛋白抗体(抗 histone)
靶抗原
细胞核内组蛋白(H1、H2A、H2B、H3、H4),是核小体的核心蛋白成分。
临床关联
主要关联药物诱导的狼疮(DIL,如普鲁卡因胺、异烟肼所致),阳性率达 90% 以上;在特发性 SLE 中阳性率约 20%~50%,也可见于类风湿关节炎。
检测意义
区分药物诱导性狼疮与特发性 SLE 的重要指标 ——DIL 患者多仅抗组蛋白阳性,而特发性 SLE 常合并其他抗核抗体阳性。
6. 抗 Sm 抗体
靶抗原
细胞核内 U1、U2、U4~U6 小核核糖核蛋白(snRNP),核心抗原为 B/B'、D1~D3 蛋白。
临床关联
SLE 的 “特异性抗体”,特异性达 99%,阳性率约 20%~40%,与 SLE 的神经系统受累(如神经精神狼疮)、肾脏受累相关。
检测意义
即使抗 dsDNA 阴性,抗 Sm 阳性仍可确诊 SLE,是 SLE 诊断的 “金标准” 之一,且抗体滴度与病情活动度无明显关联,阳性多提示疾病确诊。
7. 抗干燥综合征 A 抗原抗体(抗 SSA/Ro)
靶抗原
细胞核内 Ro 小核糖核蛋白(含 60kD 和 52kD 蛋白亚型),可与 RNA 结合形成复合物。
临床关联
干燥综合征(阳性率 60%~70%)、SLE(阳性率 30%~50%)的核心抗体,尤其与 SLE 的光敏反应、新生儿狼疮综合征(NLE)密切相关 ——NLE 患儿母亲多为抗 SSA 阳性,可导致胎儿心脏传导阻滞。
检测意义
对干燥综合征的诊断(2016 年 EULAR/ACR 分类标准)至关重要,也是预测 SLE 患者光敏反应、新生儿狼疮风险的关键指标。
8. 抗干燥综合征 B 抗原抗体(抗 SSB/La)
靶抗原
细胞核内 La 小核糖核蛋白(48kD 蛋白),参与 RNA 聚合酶 Ⅲ 的转录过程。
临床关联
干燥综合征的特异性抗体(特异性约 90%),阳性率约 40%~60%,常与抗 SSA 同时阳性;在 SLE 中阳性率约 10%~20%,与唾液腺、泪腺等外分泌腺损伤程度相关。
检测意义
抗 SSB 阳性提示干燥综合征诊断明确,且患者外分泌腺功能损伤多较严重,需加强口干、眼干症状的干预。
9. 抗核糖核蛋白抗体(抗 nRNP/U1-RNP)
靶抗原
细胞核内 U1 小核核糖核蛋白(含 70kD、A、C 蛋白亚型),参与 mRNA 的剪接过程。
临床关联
混合性结缔组织病(MCTD)的 “标志性抗体”,阳性率达 95%~100%,且多为高滴度阳性;在 SLE 中阳性率约 30%~40%,与雷诺现象、手指肿胀等症状相关。
检测意义
高滴度抗 nRNP 阳性 + 雷诺现象 + 关节痛,高度提示 MCTD;在 SLE 中阳性多提示病情相对稳定,肾脏受累风险较低。
10. 抗核糖体 P 蛋白抗体(抗 rRNP)
靶抗原
细胞质内核糖体大亚基的 P0、P1、P2 蛋白,参与蛋白质合成。
临床关联
SLE 的特异性抗体(特异性约 95%),阳性率约 10%~30%,与神经精神狼疮(如癫痫、认知障碍)、肝脏受累(狼疮肝炎)密切相关。
检测意义
抗 rRNP 阳性是 SLE 患者发生神经精神症状的独立危险因素,需密切监测神经系统体征,及时干预。
11. 抗增殖细胞核抗原抗体(抗 PCNA)
靶抗原
细胞核内增殖细胞核抗原(36kD 蛋白),参与 DNA 复制与修复。
临床关联
SLE 的特异性抗体(特异性约 90%),阳性率约 2%~10%,与 SLE 的皮肤病变(如蝶形红斑)、肾脏受累相关。
检测意义
临床少见,但阳性多提示 SLE 诊断明确,且病情活动度较高,需加强随访。
12. 抗着丝点抗体(抗 ACA/CENP-B)
靶抗原
细胞核内着丝粒蛋白 B(80kD 蛋白),参与细胞分裂时染色体的排列与分离。
临床关联
局限性系统性硬化症(CREST 综合征:钙质沉着、雷诺现象、食管运动障碍、指端硬化、毛细血管扩张)的标志性抗体,阳性率约 80%~90%;也可见于干燥综合征、原发性胆汁性胆管炎(PBC)。
检测意义
抗 ACA 阳性提示硬皮病类型为局限性,患者肺间质病变、肾脏危象风险较低,预后较好。
13. 抗核纤层蛋白 B1 抗体(抗 lamin B1)
靶抗原
细胞核膜内层的核纤层蛋白 B1(67kD 蛋白),维持核膜结构稳定。
临床关联
多见于系统性硬化症(阳性率约 10%~20%),也与自身免疫性肝炎、干燥综合征相关,与患者的皮肤硬化程度、食管受累相关。
检测意义
辅助判断系统性硬化症的器官受累范围,阳性患者需关注食管动力障碍(如吞咽困难)。
14. 抗拓扑异构酶 Ⅰ 抗体(抗 Scl-70)
靶抗原
细胞核内拓扑异构酶 Ⅰ(100kD 蛋白),参与 DNA 的解旋与复制。
临床关联
弥漫型系统性硬化症的标志性抗体(特异性约 90%),阳性率约 20%~40%,与肺间质病变、弥漫性皮肤硬化、肾脏危象密切相关。
检测意义
抗 Scl-70 阳性提示硬皮病类型为弥漫型,患者肺间质纤维化、肾衰竭风险较高,需定期进行胸部 CT、肾功能监测。
15. 抗 PM-Scl 抗体(抗 PM-1)
靶抗原
细胞核仁内的 PM-Scl 复合物(含 11 种蛋白亚型,以 75kD 和 100kD 为主),参与核糖体的组装。
临床关联
多见于多发性肌炎 / 皮肌炎(PM/DM)与系统性硬化症的重叠综合征(阳性率约 10%~20%),也可见于单纯性多发性肌炎(阳性率约 5%~10%)。
检测意义
阳性提示重叠综合征,患者多表现为肌肉炎症(如肌无力、肌酶升高)合并皮肤硬化,治疗需兼顾免疫抑制与对症支持。
抗细胞浆 / 细胞膜抗体(12 种):血管炎与器官特异性肝病的关键指标
此类抗体针对细胞浆内酶、蛋白复合物或细胞膜表面受体,主要关联系统性血管炎、自身免疫性肝病、肾病综合征等疾病,是明确疾病亚型、判断预后的重要依据。
1. 抗中性粒细胞胞浆抗体(c-ANCA / 抗 PR3)
靶抗原
中性粒细胞胞浆内的蛋白酶 3(PR3,29kD 蛋白),是中性粒细胞活化后释放的炎症蛋白酶。
临床关联
肉芽肿性多血管炎(GPA,原韦格纳肉芽肿)的标志性抗体,阳性率约 80%~90%,尤其在活动性 GPA 中阳性率更高;也可见于显微镜下多血管炎(MPA)、嗜酸性肉芽肿性多血管炎(EGPA)。
检测意义
c-ANCA 阳性 + 上呼吸道 / 肺部病变(如鼻窦炎、肺结节)+ 肾脏受累(如血尿、蛋白尿),高度提示 GPA;抗体滴度与疾病活动度相关,滴度下降提示治疗有效。
2. 抗髓过氧化物酶抗体(p-ANCA / 抗 MPO)
靶抗原
中性粒细胞胞浆内的髓过氧化物酶(MPO,146kD 蛋白),参与活性氧的生成,介导炎症反应。
临床关联
显微镜下多血管炎(MPA,阳性率约 60%~80%)、嗜酸性肉芽肿性多血管炎(EGPA,阳性率约 40%~60%)的核心抗体,也与特发性新月体性肾小球肾炎(急进性肾炎)密切相关。
检测意义
p-ANCA 阳性 + 急进性肾功能衰竭 + 肺出血,需高度怀疑 MPO 相关性血管炎,需紧急启动免疫抑制治疗(如激素联合环磷酰胺)。
3. 抗嗜天青颗粒抗体(抗 AZU)
靶抗原
中性粒细胞胞浆内的嗜天青颗粒蛋白(天青杀素,37kD 蛋白),具有抗菌、抗炎作用。
临床关联
多见于显微镜下多血管炎(阳性率约 10%~20%)、肉芽肿性多血管炎(阳性率约 5%~10%),特异性较低,常与抗 MPO 或抗 PR3 同时阳性。
检测意义
辅助判断血管炎的炎症活动度,单独阳性临床价值有限,需结合其他 ANCA 亚型判断。
4. 抗弹性蛋白酶抗体(抗 ELA)
靶抗原
中性粒细胞胞浆内的弹性蛋白酶(29kD 蛋白),可降解弹性纤维,参与组织损伤。
临床关联
系统性血管炎(如 MPA、GPA)、慢性阻塞性肺疾病(COPD)急性加重期,阳性率约 15%~25%。
检测意义
在 ANCA 阴性的血管炎患者中,抗 ELA 阳性可辅助诊断,提示中性粒细胞介导的炎症损伤。
5. 抗线粒体抗体(AMA,以 AMA-M2 为主)
靶抗原
线粒体膜上的酶复合物,其中 M2 亚型靶抗原为丙酮酸脱氢酶复合物(PDHC),是临床最常见亚型。
临床关联
原发性胆汁性胆管炎(PBC,原原发性胆汁性肝硬化)的标志性抗体,AMA-M2 阳性率约 90%~95%,特异性约 95%;也可见于自身免疫性肝炎(AIH,阳性率约 10%~20%)。
检测意义
AMA-M2 阳性 + 碱性磷酸酶(ALP)升高 + 胆汁淤积症状(如黄疸、瘙痒),可确诊 PBC,是 PBC 诊断(2022 年 AASLD 指南)的核心指标。
6. 抗平滑肌抗体(抗 SMA)
靶抗原
平滑肌细胞内的肌动蛋白(如 α- 平滑肌肌动蛋白、肌钙蛋白),也可与内皮细胞、成纤维细胞的肌动蛋白反应。
临床关联
自身免疫性肝炎(AIH,阳性率约 70%~90%)的核心抗体,尤其在 Ⅰ 型 AIH 中阳性率最高;也可见于原发性胆汁性胆管炎(PBC,阳性率约 20%~30%)、慢性活动性肝炎。
检测意义
抗 SMA 阳性 + 谷丙转氨酶(ALT)升高 + 高丙种球蛋白血症,高度提示 AIH,需结合肝穿刺活检明确诊断。
7. 抗肝肾微粒体抗体(抗 LKM-1、抗 LKM-2、抗 LKM-3)
靶抗原
LKM-1 亚型靶抗原为肝细胞微粒体中的细胞色素 P450 2D6(CYP2D6),LKM-2 为 CYP2C9,LKM-3 为 UDP - 葡萄糖醛酸转移酶。
临床关联
LKM-1 多见于 Ⅱ 型自身免疫性肝炎(AIH,阳性率约 90%),患者多为年轻女性,病情进展较快;LKM-2 与药物诱导性肝炎相关;LKM-3 与慢性丁型肝炎、AIH 重叠综合征相关。
检测意义
LKM-1 阳性是 Ⅱ 型 AIH 的确诊依据,提示患者对激素治疗敏感,但易复发,需长期维持治疗。
8. 抗可溶性肝抗原抗体(抗 SLA/LP)
靶抗原
肝细胞溶质中的可溶性肝抗原 / 肝胰抗原(SLA/LP,50kD 蛋白),本质为谷胱甘肽 S - 转移酶。
临床关联
自身免疫性肝炎(AIH,阳性率约 10%~30%)的特异性抗体(特异性约 98%),尤其在 AMA、抗 SMA 阴性的 AIH 患者中阳性率较高(约 40%)。
检测意义
抗 SLA/LP 阳性提示 AIH 诊断明确,患者多表现为严重的肝炎症(如肝衰竭风险高),需积极免疫抑制治疗。
9. 抗肝细胞溶质抗原 Ⅰ 型抗体(抗 LC-1)
靶抗原
肝细胞溶质中的细胞色素 P450 2A6(CYP2A6),参与药物代谢与激素合成。
临床关联
Ⅱ 型自身免疫性肝炎(AIH,阳性率约 40%~60%),常与抗 LKM-1 同时阳性,提示病情更严重,肝纤维化进展更快。
检测意义
抗 LC-1 阳性可作为 Ⅱ 型 AIH 的补充诊断指标,阳性患者需更密切监测肝纤维化程度(如肝弹性成像)。
10. 抗肾小球基底膜抗体(抗 GBM)
靶抗原
肾小球基底膜中的 Ⅳ 型胶原蛋白 α3 链(α3 (IV) C),是基底膜的结构蛋白。
临床关联
Goodpasture 综合征(肺出血 - 肾炎综合征)的标志性抗体,阳性率约 90%~95%,可导致急进性肾小球肾炎(RPGN)、肺出血(如咯血、呼吸困难)。
检测意义
抗 GBM 阳性是 Goodpasture 综合征的确诊依据,需紧急治疗(如血浆置换 + 激素 + 环磷酰胺),否则可在数周内进展为终末期肾病。
11. 抗磷脂酶 A2 受体抗体(抗 PLA2R)
靶抗原
肾小球足细胞表面的磷脂酶 A2 受体(PLA2R,180kD 蛋白),参与肾小球滤过屏障的维持。
临床关联
特发性膜性肾病(IMN)的核心抗体,阳性率约 70%~80%,抗体滴度与蛋白尿水平、疾病活动度直接相关。
检测意义
抗 PLA2R 阳性可确诊 IMN,无需肾穿刺活检;滴度下降提示治疗有效(如利妥昔单抗治疗后),是监测疗效的关键指标。
12. 抗水通道蛋白 4 抗体(抗 AQP4)
靶抗原
中枢神经系统(如视神经、脊髓)星形胶质细胞表面的水通道蛋白 4(AQP4),参与水分子转运。
临床关联
视神经脊髓炎谱系疾病(NMOSD)的标志性抗体,阳性率约 60%~80%,与视神经炎(视力下降)、脊髓炎(肢体无力、大小便障碍)密切相关。
检测意义
抗 AQP4 阳性是 NMOSD 的确诊依据,与多发性硬化(MS)鉴别关键 ——NMOSD 患者多为抗 AQP4 阳性,MS 患者多为阴性,治疗方案完全不同。
自身抗体在免疫病理学中的作用10.1038/s41581-023-00720-1
器官特异性自身抗体(18 种):单一器官自身免疫病的诊断核心
此类抗体仅针对特定器官的组织成分,不与其他器官交叉反应,直接关联甲状腺、胰岛、胃肠道、神经肌肉等单一器官的自身免疫病,是疾病早期诊断、病因鉴别、病情监测的 “特异性工具”。
(1)甲状腺相关自身抗体(4 种)
1. 抗甲状腺过氧化物酶抗体(抗 TPO)
靶抗原
甲状腺滤泡上皮细胞内的甲状腺过氧化物酶(TPO,107kD 蛋白),参与甲状腺激素(T3、T4)的合成。
临床关联
桥本甲状腺炎(慢性淋巴细胞性甲状腺炎)的标志性抗体,阳性率约 90%~95%,是甲状腺功能减退(甲减)的最常见病因;也可见于 Graves 病(阳性率约 50%~70%)。
检测意义
抗 TPO 阳性 + 甲状腺功能减退(TSH 升高、FT4 降低),可确诊桥本甲状腺炎;即使甲状腺功能正常,高滴度抗 TPO 也提示未来发生甲减的风险较高(每年约 5% 进展为甲减)。
2. 抗甲状腺球蛋白抗体(抗 Tg)
靶抗原
甲状腺滤泡内的甲状腺球蛋白(Tg,660kD 蛋白),是甲状腺激素合成的前体蛋白。
临床关联
桥本甲状腺炎(阳性率约 60%~80%)、甲状腺乳头状癌(PTC)术后监测,PTC 患者术后抗 Tg 阳性提示肿瘤残留或复发风险较高。
检测意义
单独抗 Tg 阳性临床价值有限,常与抗 TPO 同时阳性,辅助桥本甲状腺炎诊断;PTC 术后需结合 Tg 蛋白水平(而非仅抗体)判断复发 —— 若 Tg 蛋白升高 + 抗 Tg 阳性,需进一步排查转移。
3. 抗 TSH 受体抗体(抗 TRAb,含刺激性、阻断性亚型)
靶抗原
甲状腺滤泡上皮细胞表面的促甲状腺激素(TSH)受体,调节甲状腺激素合成与释放。
临床关联
刺激性 TRAb(TSAb)关联 Graves 病(毒性弥漫性甲状腺肿),阳性率约 80%~90%,导致甲状腺激素过度合成(甲亢,如心悸、多汗、体重下降);阻断性 TRAb(TBAb)关联桥本甲状腺炎,导致甲状腺激素合成减少(甲减)。
检测意义
刺激性 TRAb 阳性是 Graves 病的确诊依据,与甲亢病情活动度相关;Graves 病患者治疗后 TRAb 转阴,提示可停药且复发风险低(<10%)。
4. 抗甲状腺微粒体抗体(抗 TMA)
靶抗原
甲状腺滤泡上皮细胞的微粒体成分,本质与抗 TPO 的靶抗原重叠(均为 TPO),是早期检测 TPO 抗体的 “旧称”。
临床关联
与抗 TPO 完全一致,多见于桥本甲状腺炎、Graves 病,目前临床已多被抗 TPO 检测取代。
检测意义
临床价值与抗 TPO 相同,仅在部分老旧检测方法中使用,阳性结果需等同于抗 TPO 阳性解读。
(2)胰岛相关自身抗体(3 种)
1. 抗胰岛素抗体(抗 Ins)
靶抗原
胰岛 β 细胞分泌的胰岛素(5.8kD 蛋白),是调节血糖的关键激素。
临床关联
1 型糖尿病(T1DM,阳性率约 40%~60%),尤其在疾病早期或儿童 T1DM 中阳性率较高;也可见于胰岛素自身免疫综合征(IAS,患者无糖尿病却出现低血糖,因抗体与胰岛素结合后突然释放)、2 型糖尿病(T2DM)使用外源性胰岛素后(产生的 “治疗性抗体”)。
检测意义
未使用胰岛素的患者抗 Ins 阳性,高度提示 T1DM 或 IAS;T2DM 患者使用胰岛素后抗 Ins 阳性,若出现血糖波动(如低血糖),需调整胰岛素类型(如换用胰岛素类似物)。
2. 抗谷氨酸脱羧酶抗体(抗 GAD65)
靶抗原
胰岛 β 细胞内的谷氨酸脱羧酶 65 亚型(GAD65,65kD 蛋白),参与 γ- 氨基丁酸(GABA)的合成。
临床关联
1 型糖尿病(T1DM,阳性率约 70%~90%),是 T1DM 早期诊断的核心指标(甚至在血糖升高前数年即可阳性);也关联僵人综合征(SPS,阳性率约 80%,患者表现为肌肉僵硬、痉挛)。
检测意义
成人隐匿性自身免疫性糖尿病(LADA,“缓慢进展型 T1DM”)的关键诊断指标 ——LADA 患者初期表现类似 T2DM,但抗 GAD65 阳性,需尽早使用胰岛素治疗,避免 β 细胞过度损伤。
3. 抗胰岛细胞抗体(抗 ICA / 抗 IA-2)
靶抗原
抗 ICA 靶抗原为胰岛 β 细胞的多种胞浆蛋白(无特异性),抗 IA-2 靶抗原为胰岛 β 细胞内的酪氨酸磷酸酶(IA-2,105kD 蛋白),目前临床多检测抗 IA-2(特异性更高)。
临床关联
1 型糖尿病(T1DM,抗 IA-2 阳性率约 50%~70%),尤其在儿童 T1DM 中阳性率更高;抗 IA-2 阳性与胰岛 β 细胞功能衰竭速度相关,阳性患者 β 细胞功能下降更快。
检测意义
抗 GAD65 + 抗 IA-2 双阳性,提示 T1DM 诊断明确,且未来胰岛 β 细胞功能衰竭风险极高,需终身依赖胰岛素治疗。
(3)胃肠道相关自身抗体(4 种)
1. 抗胃壁细胞抗体(抗 PCA)
靶抗原
胃壁主细胞、壁细胞表面的蛋白(如 H+/K+-ATP 酶),壁细胞参与胃酸分泌,主细胞分泌胃蛋白酶原。
临床关联
慢性萎缩性胃炎(A 型胃炎,胃体为主)的标志性抗体,阳性率约 80%~90%;也与恶性贫血(因胃酸缺乏导致维生素 B12 吸收障碍)密切相关。
检测意义
抗 PCA 阳性提示胃体黏膜萎缩,需进一步检测胃泌素水平、维生素 B12 水平,避免因长期维生素 B12 缺乏导致巨幼细胞性贫血、神经系统损伤(如周围神经病变)。
2. 抗内因子抗体(抗 IF)
靶抗原
胃壁壁细胞分泌的内因子(55kD 蛋白),与维生素 B12 结合形成复合物,促进其在回肠吸收。
临床关联
恶性贫血的特异性抗体(特异性约 95%),阳性率约 60%~70%,是维生素 B12 吸收障碍的直接原因 —— 抗 IF 与内因子结合,阻止其与维生素 B12 结合,导致缺乏。
检测意义
抗 IF 阳性可确诊恶性贫血,无需胃镜活检;患者需终身补充维生素 B12(如肌内注射甲钴胺),否则可导致不可逆的神经系统损伤(如记忆力下降、肢体麻木)。
3. 抗麦胶蛋白抗体(抗 AGA)
靶抗原
小麦、大麦、黑麦中的麦胶蛋白(醇溶蛋白),是乳糜泻(腹腔疾病)的关键致病抗原。
临床关联
乳糜泻的筛查指标,阳性率约 70%~80%,患者摄入麦胶后出现腹泻、腹痛、体重下降、营养不良(如缺铁性贫血、骨质疏松)。
检测意义
抗 AGA 阳性需进一步检测抗肌内膜抗体(抗 EMA)或抗组织转谷氨酰胺酶抗体(抗 tTG),并结合小肠黏膜活检确诊;确诊后需严格无麦胶饮食,症状可迅速缓解。
4. 抗肌内膜抗体(抗 EMA)
靶抗原
小肠黏膜上皮细胞的肌内膜蛋白(主要为肌动蛋白),是乳糜泻的特异性标志物。
临床关联
乳糜泻的确诊指标之一,阳性率约 80%~90%,特异性约 95%,与小肠黏膜绒毛萎缩程度相关 —— 抗体阳性患者多存在中重度绒毛萎缩。
检测意义
抗 EMA 阳性 + 无麦胶饮食后症状改善,可临床诊断乳糜泻,减少小肠活检的需求;尤其适用于儿童或无法耐受活检的患者。
(4)神经肌肉相关自身抗体(4 种)
1. 抗乙酰胆碱受体抗体(抗 AChR)
靶抗原
神经肌肉接头(突触后膜)的乙酰胆碱受体(AChR),参与神经冲动向肌肉的传递。
临床关联
重症肌无力(MG)的标志性抗体,阳性率约 80%~90%(全身型 MG 阳性率更高,眼肌型约 50%),患者表现为波动性肌无力(如眼睑下垂、肢体无力、吞咽困难),活动后加重、休息后缓解。
检测意义
抗 AChR 阳性是 MG 的确诊依据,与疾病严重程度相关;治疗后抗体滴度下降提示病情改善,是监测疗效的关键指标。
2. 抗肌联蛋白抗体(抗 Titin)
靶抗原
骨骼肌细胞内的肌联蛋白(Titin,3000kD 蛋白),是骨骼肌的结构蛋白,维持肌肉收缩功能。
临床关联
重症肌无力(MG)合并胸腺瘤的特异性抗体,阳性率约 80%~90%(无胸腺瘤的 MG 患者阳性率仅约 10%),与 MG 的严重程度(如呼吸肌受累)相关。
检测意义
抗 Titin 阳性提示 MG 患者合并胸腺瘤的风险极高,需紧急进行胸部 CT 检查;胸腺瘤切除后抗体滴度下降,提示病情缓解。
3. 抗电压门控钙通道抗体(抗 VGCC)
靶抗原
神经肌肉接头(突触前膜)的电压门控钙通道(VGCC),参与乙酰胆碱的释放。
临床关联
Lambert-Eaton 肌无力综合征(LEMS)的标志性抗体,阳性率约 80%~90%,多与小细胞肺癌(SCLC)相关(约 50% 的 LEMS 患者合并 SCLC),患者表现为下肢近端肌无力、自主神经症状(如口干、便秘)。
检测意义
抗 VGCC 阳性提示 LEMS,需进一步排查小细胞肺癌(如胸部 CT、肿瘤标志物);若为肿瘤相关性 LEMS,肿瘤治疗后肌无力症状可缓解。
4. 抗 Yo 抗体(抗 Purkinje 细胞抗体)
靶抗原
小脑 Purkinje 细胞内的 Yo 蛋白(CDR2 蛋白),参与小脑的运动协调功能。
临床关联
副肿瘤性小脑变性(PCD)的标志性抗体,多与妇科肿瘤(如卵巢癌、乳腺癌)相关,患者表现为急性或亚急性小脑功能障碍(如步态不稳、共济失调、眼球震颤)。
检测意义
抗 Yo 阳性提示副肿瘤综合征,需紧急排查妇科肿瘤;即使肿瘤早期无症状,也需定期随访(如妇科超声、肿瘤标志物 CA125),肿瘤治疗后小脑症状可部分改善。
(5)其他器官相关自身抗体(3 种)
1. 抗视网膜抗体(抗 retina)
靶抗原
视网膜感光细胞(如视杆细胞、视锥细胞)的蛋白成分(如恢复蛋白、转导蛋白)。
临床关联
副肿瘤性视网膜病变(如癌症相关性视网膜病变、黑色素瘤相关性视网膜病变),多与小细胞肺癌、黑色素瘤相关,患者表现为进行性视力下降、视野缺损。
检测意义
抗视网膜抗体阳性提示副肿瘤性视网膜病变,需排查原发肿瘤;早期肿瘤治疗可延缓视力下降,否则可进展为失明。
2. 抗精子抗体(抗 AsAb)
靶抗原
精子表面的多种蛋白(如精子头部的顶体蛋白、尾部的鞭毛蛋白)。
临床关联
男性免疫性不育(约占男性不育的 10%~20%),抗 AsAb 与精子结合后,可抑制精子活力、阻止精子与卵子结合;也可见于女性免疫性不孕(抗体通过宫颈黏液与精子结合)。
检测意义
不孕夫妇排查时,抗 AsAb 阳性提示免疫性不孕,治疗需采用避孕套隔绝疗法(减少抗体产生)或辅助生殖技术(如试管婴儿)。
3. 抗心肌抗体(抗 AMA)
靶抗原
心肌细胞内的多种蛋白(如肌动蛋白、肌钙蛋白、线粒体蛋白)。
临床关联
病毒性心肌炎(如柯萨奇病毒、新冠病毒感染后)、扩张型心肌病(DCM)、风湿热,阳性率约 30%~50%,与心肌炎症损伤程度相关。
检测意义
抗 AMA 阳性 + 心肌酶升高(如 CK-MB、肌钙蛋白)+ 心电图异常,提示心肌炎症,需进一步进行心脏超声、心肌活检明确诊断,避免进展为心力衰竭。
四、其他关联自身抗体(5 种):类风湿关节炎与抗磷脂综合征的关键标志物
此类抗体虽不局限于单一系统或器官,但主要关联类风湿关节炎、抗磷脂综合征等特定疾病,是疾病诊断、病情评估、预后判断的核心指标,临床应用广泛。
1. 抗环瓜氨酸肽抗体(抗 CCP)
靶抗原
关节软骨中的环瓜氨酸化肽(含瓜氨酸残基的蛋白,如波形蛋白、纤维蛋白原),是类风湿关节炎(RA)的特异性自身抗原。
临床关联
类风湿关节炎的早期诊断抗体,阳性率约 60%~70%,特异性约 95%,可在 RA 症状出现前数年阳性;与 RA 的关节骨侵蚀风险密切相关 —— 抗 CCP 阳性患者骨侵蚀发生率是阴性患者的 3~5 倍。
检测意义
抗 CCP 阳性 + 类风湿因子(RF)阳性 + 关节肿痛,可早期确诊 RA,即使不符合 RA 分类标准(如关节数不足),也需密切随访;阳性患者需尽早使用改善病情抗风湿药(DMARDs,如甲氨蝶呤),预防骨侵蚀。
2. 抗角蛋白抗体(抗 AKA)
靶抗原
大鼠食管上皮细胞的角蛋白(主要为角蛋白 18、19),与 RA 患者关节内的环瓜氨酸化蛋白交叉反应。
临床关联
类风湿关节炎的特异性抗体,阳性率约 30%~50%,特异性约 90%,常与抗 CCP 同时阳性;与 RA 的关节畸形、骨侵蚀风险相关。
检测意义
抗 AKA 阳性可辅助 RA 诊断,尤其在抗 CCP 阴性的 RA 患者中(约 10%~20%),可补充诊断价值;阳性患者需加强关节影像学监测(如 X 线、超声)。
3. 抗心磷脂抗体(抗 ACA,含 IgG、IgM、IgA 亚型)
靶抗原
细胞膜表面的磷脂(如心磷脂、磷脂酰胆碱),与 β2 - 糖蛋白 Ⅰ(β2-GP1)结合后被识别。
临床关联
抗磷脂综合征(APS)的核心抗体,IgG 亚型阳性率约 70%~80%,IgM 亚型约 50%~60%;与血栓形成(如深静脉血栓、肺栓塞、脑卒中)、反复流产(妊娠 10 周后流产)、血小板减少密切相关。
检测意义
抗 ACA 阳性(尤其 IgG 高滴度)+ 血栓 / 流产史,可确诊 APS;需长期使用抗凝治疗(如低分子肝素、华法林),预防血栓复发。
4. 抗 β2 - 糖蛋白 Ⅰ 抗体(抗 β2-GP1)
靶抗原
血浆中的 β2 - 糖蛋白 Ⅰ(β2-GP1,50kD 蛋白),是抗磷脂抗体的辅助因子,与磷脂结合后形成复合物。
临床关联
抗磷脂综合征(APS)的特异性抗体,阳性率约 60%~70%,特异性约 90%,比抗 ACA 更能预测血栓风险 —— 抗 β2-GP1 阳性患者血栓复发率更高。
检测意义
抗 β2-GP1 阳性 + 抗 ACA 阳性,提示 APS 诊断明确,且血栓风险极高;即使抗 ACA 阴性,抗 β2-GP1 阳性仍可确诊 APS(约 10% 的 APS 患者仅抗 β2-GP1 阳性)。
5. 抗 RA33 抗体(抗 hnRNP A2)
靶抗原
细胞核内的异质性核核糖核蛋白 A2(hnRNP A2,33kD 蛋白),参与 mRNA 的加工与转运。
临床关联
类风湿关节炎(RA)的早期抗体,阳性率约 20%~40%,尤其在 RA 发病前 1~2 年即可阳性;也可见于系统性红斑狼疮(SLE,阳性率约 10%~20%)、干燥综合征。
检测意义
抗 RA33 阳性可辅助 RA 早期诊断,尤其在 RF、抗 CCP 阴性的早期 RA 患者中(约 15%),可补充诊断价值;但特异性较低,需结合临床症状判断。
* 内容供参考,诊断治疗请遵医嘱。
参考资料
Cardozo T, Cardozo L and Boutjdir M (2022) Autoantibody: Autoantigen Competitor Decoys: Application to Cardiac Phenotypes. Front. Immunol. 13:812649. doi: 10.3389/fimmu.2022.812649
Autoantibody Biomarkers in Rheumatic Diseases,Int. J. Mol. Sci. 2020, 21, 1382; doi:10.3390/ijms21041382
Fritzler MJ, Choi MY, Satoh M and Mahler M (2021) Autoantibody Discovery, Assay Development and Adoption: Death Valley, the Sea of Survival and Beyond. Front. Immunol. 12:679613. doi: 10.3389/fimmu.2021.679613