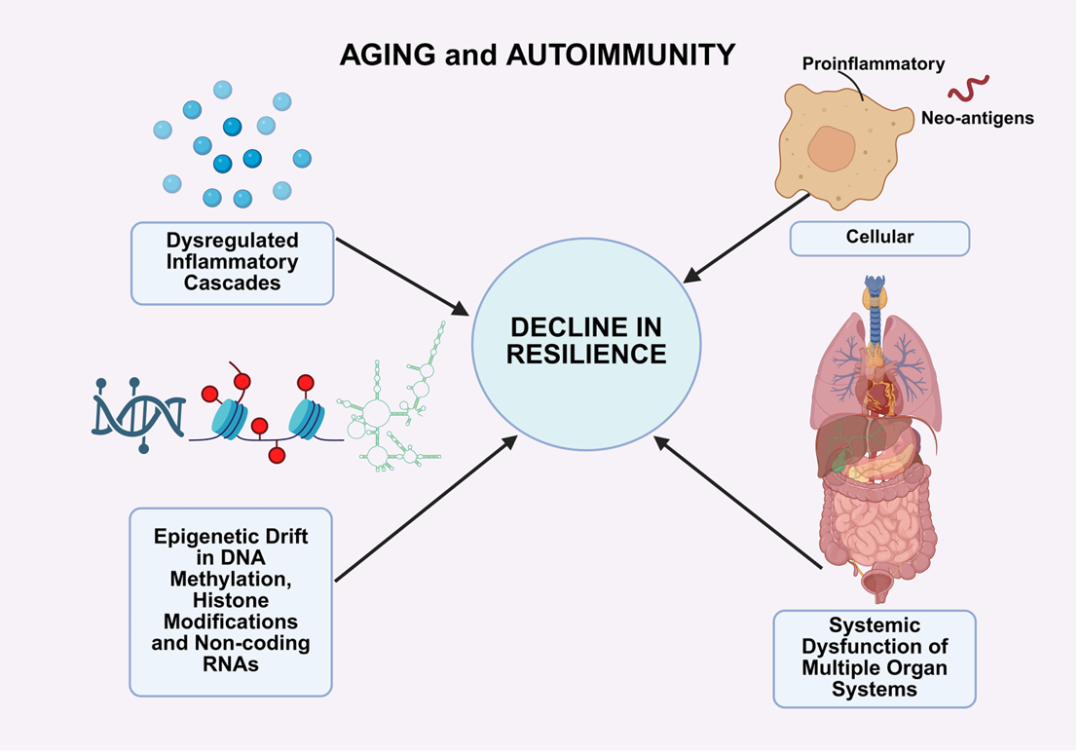
免疫系统是机体抵御病原体、清除癌变细胞、维持组织稳态的核心防线,由先天免疫与适应性免疫两大分支协同构成,涉及免疫器官、免疫细胞、细胞因子、信号通路等多层级调控网络。随着年龄增长,这一网络会发生持续性、不可逆的重塑,整体功能呈现下降趋势,即免疫衰老。
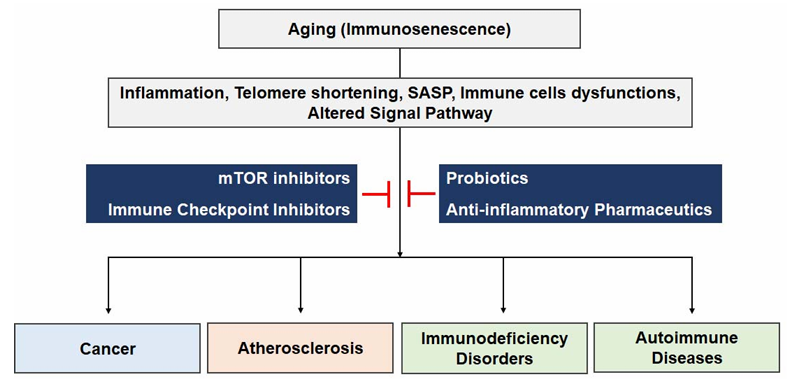
10.3390/ijms242115584
免疫衰老典型特征
免疫衰老的典型特征具有高度一致性:首先,免疫器官退化,胸腺作为 T 细胞发育成熟的核心场所,会在青春期后逐渐发生胸腺萎缩,导致初始 T 细胞生成数量大幅减少,T 细胞受体库多样性显著降低,机体对新抗原的识别与应答能力大幅下降。其次,免疫细胞数量与功能失衡,抗原呈递细胞(如树突状细胞、巨噬细胞)的抗原摄取、加工与呈递效率降低;T 淋巴细胞中,初始 CD8+T 细胞减少,记忆表型细胞比例上升,共刺激分子 CD28、CD27 表达下降,细胞毒性与增殖能力减弱;B 淋巴细胞数量减少,分化为浆细胞的能力受阻,抗体生成量降低、亲和力下降,体液免疫防御功能显著弱化。最后,炎症稳态被打破,衰老免疫细胞会大量释放促炎因子、趋化因子、生长因子等活性物质,形成衰老相关分泌表型(SASP),引发全身低度慢性炎症,这种慢性炎症又会进一步加速免疫细胞衰老,形成恶性循环。
免疫衰老并非单一的功能减退,而是免疫监视、免疫防御、免疫自稳三大功能全面失调的结果。
免疫衰老引发的四大类疾病
肿瘤
肿瘤是老年人最主要的死亡原因之一,年龄是肿瘤发生的最强危险因素,其核心诱因正是免疫衰老导致的肿瘤免疫监视功能崩溃。
正常情况下,免疫系统能够识别并清除体内突变的癌细胞,这一过程被称为 “癌症免疫编辑”,而免疫衰老则彻底打破了这一平衡。一方面,老年人的抗原呈递细胞功能衰退,无法有效将肿瘤抗原呈递给 T 细胞,导致抗肿瘤免疫启动受阻;初始 T 细胞数量不足、受体多样性降低,使得机体难以识别新型肿瘤抗原,无法形成有效的特异性杀伤。另一方面,衰老的免疫微环境会促进免疫抑制细胞富集,肿瘤组织会分泌趋化因子招募调节性 T 细胞(Tregs),并激活髓系来源抑制细胞,这类细胞会直接抑制细胞毒性 T 细胞、NK 细胞的功能,营造免疫抑制性肿瘤微环境。此外,衰老相关的慢性炎症会持续释放 IL-6、TNF-α 等促炎因子,这些因子既能促进癌细胞增殖、侵袭与转移,又能进一步抑制免疫细胞功能,形成 “炎症 — 免疫抑制 — 肿瘤进展” 的恶性循环。
临床与基础研究均证实,老年肿瘤患者的免疫检查点分子(如 PD-1、CTLA-4)表达水平更高,T 细胞耗竭与衰老更显著,对传统治疗与免疫治疗的响应率更低,预后更差。这也意味着,肿瘤的发生不仅是细胞突变的结果,更是免疫衰老驱动的免疫监视失效所导致的最终产物。
动脉粥样硬化
动脉粥样硬化是心血管疾病的核心病理基础,衰老是其不可调控的首要危险因素,而免疫衰老介导的慢性炎症与免疫失衡,是动脉粥样硬化发生、发展的核心驱动力。
动脉粥样硬化的本质是血管壁的慢性炎症性疾病,免疫细胞在其中扮演关键角色。衰老状态下,血管壁内的巨噬细胞、树突状细胞、T 细胞均会发生衰老,大量释放 SASP 因子,包括 IL-6、IL-8、CCL2、CCL20 等,这些因子会招募更多免疫细胞聚集在血管内皮下,促进脂质沉积、泡沫细胞形成与斑块生长。同时,衰老 T 细胞会异常激活 p38 MAPK 信号通路,大量分泌 IFN-γ,加剧血管壁炎症与斑块不稳定,提升斑块破裂、血栓形成的风险,进而引发心肌梗死、脑梗死等致命性心脑血管事件。
更重要的是,免疫衰老会导致调节性 T 细胞(Tregs)数量减少、功能下降,免疫耐受失衡。正常情况下,Tregs 能够抑制效应 T 细胞的过度活化,减轻血管炎症;而老年人体内 Tregs / 效应 T 细胞比值显著降低,无法有效控制炎症反应,导致动脉粥样硬化病变持续进展。临床研究已证实,冠心病患者外周血 Tregs 数量明显低于健康人群,Tregs 功能缺陷程度与斑块稳定性、心血管事件风险直接相关。
免疫缺陷病
免疫缺陷是免疫衰老最直观的表现,老年人因免疫系统先天性防御能力下降,极易发生获得性免疫缺陷,而普通变异型免疫缺陷病(CVID) 则是老年人群最常见的原发性免疫缺陷病。
老年免疫缺陷的核心诱因是胸腺萎缩与淋巴细胞多样性下降。胸腺退化导致初始 T 细胞生成停滞,T 细胞受体库无法更新,对新型病原体的识别能力几乎丧失;B 细胞分化障碍,无法有效生成 IgG、IgA、IgM 等抗体,体液免疫防线崩溃。这类获得性免疫缺陷使得老年人对流感、肺炎、带状疱疹等感染高度易感,且感染后易发展为重症,病死率显著升高。
CVID 作为代表性原发性免疫缺陷,其核心特征是免疫球蛋白水平显著降低,近三分之一患者伴随 T 细胞功能缺陷,B 细胞无法分化为浆细胞,抗体生成严重不足。CVID 患者不仅反复发生感染,约 30% 会合并自身免疫病,如自身免疫性溶血性贫血、免疫性血小板减少性紫癜、血清阴性类风湿关节炎等。这一现象揭示了免疫衰老与免疫缺陷、自身免疫病之间的内在关联:免疫功能缺陷与免疫紊乱往往同时存在,共同加剧老年人群的健康风险。
自身免疫性疾病
免疫耐受的多重失守
中枢耐受缺陷
胸腺萎缩导致阴性选择失败,大量自身反应性 T 细胞逃逸至外周。
外周耐受崩溃
Treg 功能不足、共刺激信号异常(如 CD28⁻T 细胞增多),使自身反应性淋巴细胞无法被有效抑制NCBI。
自身抗原暴露
慢性炎症与组织损伤导致隐蔽自身抗原释放,被异常活化的免疫细胞识别。
细胞衰老与自身免疫的分子链接
线粒体功能障碍
衰老免疫细胞线粒体受损,ROS 过量产生,激活cGAS-STING等炎症通路,加剧自身免疫炎症。
表观遗传改变
DNA 甲基化、组蛋白修饰异常,导致免疫细胞基因表达紊乱,促进自身反应性与炎症表型PMC。
基因组不稳定
DNA 损伤累积,激活p53、STAT3等通路,破坏免疫平衡,诱发自身免疫。
免疫衰老的四大分子机制
免疫衰老并非随机发生的生理衰退,而是由端粒缩短、免疫衰老重塑、SASP 介导的慢性炎症、信号通路异常四大分子机制共同驱动的程序化过程,四大机制相互关联、协同作用,构成了免疫衰老的核心调控网络。
(一)端粒缩短:细胞衰老的 “分子时钟”
端粒是位于染色体末端的 DNA— 蛋白质复合物,其长度随细胞分裂不断缩短,是触发细胞衰老的核心分子标记,被称为细胞衰老的 “时钟”。免疫细胞的高度增殖特性,使其对端粒缩短极度敏感。
正常情况下,免疫细胞可通过上调端粒酶活性部分抵抗端粒损耗,但衰老状态下,端粒酶活性显著下降,T 细胞、B 细胞、NK 细胞等均出现谱系特异性端粒缩短。当端粒缩短至临界长度时,细胞会启动 DNA 损伤应答,触发细胞周期停滞,最终进入衰老状态。端粒缩短不仅直接导致免疫细胞增殖能力下降、寿命缩短,还会进一步促进 SASP 释放,放大慢性炎症,形成端粒缩短 — 细胞衰老 — 炎症加剧的正反馈循环。
(二)免疫衰老的系统性重塑
免疫衰老的核心是适应性免疫显著衰退,先天免疫相对保留的不对称重塑。随着年龄增长,初始 T、B 细胞数量持续减少,淋巴细胞总数下降,适应性免疫对新抗原的应答能力几乎丧失;而先天免疫细胞(如中性粒细胞、巨噬细胞)的数量与表面标记相对稳定,成为老年免疫的主要防线。
但先天免疫细胞同样会发生功能异常,中性粒细胞会通过释放活性氧(ROS)加剧端粒损伤,诱导邻近细胞衰老;中性粒细胞在衰老组织中的异常聚集,会进一步传播衰老信号,加速组织器官的免疫衰退。这种不对称重塑使得老年人的免疫防御呈现 “先天免疫勉强维持,适应性免疫全面崩溃” 的状态,是感染、肿瘤高发的核心原因。
(三)SASP:慢性炎症的核心来源
衰老细胞会大量分泌促炎细胞因子、趋化因子、生长因子、基质金属蛋白酶等物质,统称为衰老相关分泌表型(SASP),是老年慢性低度炎症的核心驱动因素。
SASP 的成分复杂,主要包括 IL-6、IL-8、TNF-α、MCP-1 等,其释放源于 DNA 损伤、线粒体功能障碍、细胞周期调控异常等上游信号。SASP 具有双重作用:生理状态下,SASP 可招募免疫细胞清除衰老细胞、促进组织修复;但在衰老机体中,SASP 持续过量释放,会破坏组织微环境,诱导邻近健康细胞衰老,促进慢性炎症、肿瘤、动脉粥样硬化等疾病发生。研究证实,将衰老免疫细胞移植到年轻小鼠体内,可诱导年轻小鼠出现全身衰老表型,而移植年轻免疫细胞则能清除衰老细胞、延缓衰老,直接证明 SASP 在免疫衰老与全身衰老中的核心作用。
(四)信号通路异常:mTOR 通路的核心调控作用
mTOR(雷帕霉素靶蛋白)通路是细胞生长、代谢、衰老的核心调控通路,其异常激活是免疫衰老的关键分子机制。mTOR 通路包括 mTORC1 与 mTORC2 两大复合物,分别调控细胞周期、自噬、代谢重编程等过程。
衰老状态下,mTORC1 通路过度激活,抑制细胞自噬,导致免疫细胞代谢紊乱、功能衰退;而 mTORC2 通路异常则影响 CD8 + 记忆 T 细胞的分化与功能。同时,衰老 T 细胞中 p38 MAPK 通路异常激活,大量分泌促炎因子,进一步加剧免疫功能异常。研究证实,使用雷帕霉素等 mTOR 抑制剂,可提升老年人疫苗接种后的抗体水平,降低 T 细胞 PD-1 表达,改善免疫功能,延长健康寿命,直接证明 mTOR 通路是干预免疫衰老的关键靶点。